SINDROMUL SJOGREN (SS)
este o boala inflamatorie autoimuna, lent
progresiva, care afecteaza tintit glandele exocrine. Este
caracterizata de prezenta unui infiltrat inflamator limfocitar la
nivelul glandelor salivare si lacrimale determinand scaderea
secretiei acestor glande, si de productia unor autoanticorpi.
Infiltratul inflamator poate afecta si alte organe determinand astfel
afectarea sistemica a acestui sindrom. Exocrinopatia poate evolua izolat
ca SS primar (SSp) sau in asociere
cu alte boli autoimune constituind SS
secundar. In acest context asocierea cea mai frecventa este
poliartrita reumatoida intalnita in peste jumatate din cazurile
de SS secundar. Mai poate aparea si in alte boli de tesut
conjunctiv (lupus eritematos sistemic, scleroza sistemica, boala
mixta de tesut conjunctiv, poli/dermatomiozita),
crioglobulinemie mixta, ciroza biliara primitiva, hepatite
autoimune, tiroidite autoimune.
Desi SS primar se caracterizeaza prin xeroftalmie
(scaderea secretiei lacrimale) si xerostomie (scaderea
secretiei salivare), manifestarile extraglandulare apar frecvent iar
acestea pot fi: articulare, gastro-intestinale, renale, hematologice, musculare,
neurologice, pulmonare, cutanate, ginecologice si vasculare. Sindromul
Sjogren are o evolutie
Henrik Sjogren este probabil cel mai cunoscut nume de origine suedeza in literatura medicala internationala, datorita sindromului ce-i poarta numele. La varsta de 20 de ani patrunde in lumea fascinanta a medicinei urmand cursurile Institutului Karolinska din Stockholm. Dupa finalizarea studiilor va opta pentru oftalmologie si va profesa in cadrul Clinicii Serafimer din Stockholm unde va castiga atat experienta clinica cat si cea in cercetarea stiintifica.
In 1929 avea sa intalneasca un pacient ce acuza uscaciunea ochilor si a gurii precum si dureri articulare. Fiecare simptom in parte era foarte bine cunoscut dar asocierea lor l-a determinat pe Sjogren sa acorde mai mult interes acestui aspect. Insa nu era el primul care observase aceasta triada, ci in urma cu 3 ani un medic francez Henri Gougerot publicase aceeasi observatie. Astfel ne explicam eponimul Gougerot- Sjogrens disease, aparut in literatura medicala in acea perioada. Eponimul va fi restrans la Sjogrens disease cu o decada mai tarziu datorita interesului profund manifestat de Sjogren fata de aceasta entitate clinica necunoscuta la acea vreme. In cadrul Clinicii Sabbatsberg va desfasura cea mai mare parte a activitatii sale clinice si stiintifice in aceasta directie. Va publica in 1930 pentru prima data in literatura medicala, notiunea de Keratoconjunctivita sicca.
O activitate de 30 de ani, atat clinica cat si stiintifica, dedicata exclusiv acestei suferinte, numarul impresionant de cazuri raportate si articole publicate i-au adus recunostinta internationala in lumea medicala pentru descoperirea lui. A fost numit membru de onoare al Asociatiei Americane de Reumatologie, a devenit membru al Colegiului Australian Royal, membru de onoare al Societatii Suedeze de Reumatologie.
Henrik Sjogren a fost un oftalmolog care a intalnit un pacient ce acuza uscaciunea ochilor si aici se putea termina totul. Insa gandirea lui deschisa pentru cercetare l-a dus la descoperirea acestei entitati clinice care mai tarziu i-a purtat numele. Etiopatogenia insa a ramas o necunoscuta pentru Sjogren. In prezent noi stim ca Sindromul Sjogren este o boala inflamatorie cronica cu substrat autoimun.
Sindromul Sjogren este o afectiune comuna afectand in medie 0,1%- 0,4% din populatia generala clasandu-se astfel pe locul doi dupa poliartrita reumatoida intre bolile autoimune sistemice. In populatia de peste 50 de ani afecteaza intre 1-2% din indivizi. Prevalenta Sindromului Sjogren rezultata in urma studiilor epidemiologice, variaza in functie de criteriile de diagnostic folosite. Astfel Criteriile Copenhaga indica o prevalenta de 8 pac. /1000 de subiecti, Criteriile San Diego 3 pac. /1000, Criteriul European 6 /1000 subiecti. In ceea ce priveste varsta si sexul, Sindromul Sjogren afecteza cu predilectie persoanele de sex feminin aflate in decada a 5-a de viata, de obicei postmenopauza. Raportul femei/ barbati (F/B) este de 9:1.
Interesul pentru relatia ipotetica dintre virusuri si autoimunitate se desfasoara de cateva decade si continua si in prezent. Infectiile virale au solicitat atentia datorita asocierii lor frecvente cu Sindromul Sjogren (SS) insa pana in momentul de fata nu s-a putut demonstra daca aceasta asociere este de cauzalitate sau pur intamplatoare. Virusurile cel mai frecvent implicate sunt cele herpetice, virusul citomegalic (CMV), Virusul Ebstein Barr (EBV), virusurile hepatitice B si C si retrovirusuri (HTLV1). Etiologia ipotetic virala se poate explica prin sediul frecvent la nivelul glandelor salivare al infectiilor latente virale.
Sindromul Sjogren se dezvolta pe baza unui raspuns imun anormal asociind un factor de mediu ubiquitar, cum este EBV (Wen S 1996). De asemenea o prevalenta mai mare a anticorpilor anti Herpes Virus Uman tip 6 (HHV6) a fost gasita la pacientii cu SS fata de populatia generala (36% vs 10%) (Biberfeld P.1988). Din potriva alte studii infirma o prevalenta mai mare a HHV6 la pacientii cu SS (Baboonian C1990). Dificultatea in evaluarea rolului viral in etiopatogenie se datoreaza si prevalentei crescute a infectiilor cu HHV6 si EBV in populatia generala.
Retrovirusurile sunt cunoscute ca agenti infectanti ai celulelor imune determinand anomalii ale sistemului imun. Titruri crescute ale anticorpilor anti HTLV1 (Human T lymphotropic Virus type1) si un nivel crescut al anticorpilor de clasa IgA anti HTLV1 s-au gasit la pacientii cu SS (Terada k 1994).
Infectia cu Virusul Hepatitic C (VHC) de asemenea a fost intalnita la 14% din cazuri (Garsia-Carrasco M 1997) iar afectarea hepatica era prezenta la toti acesti pacienti. Analizand asocierea intre sialadenita limfocitica cronica si afectarea cronica hepatica cu VHC a dovedit asemanarile histologice comune mai frecvente la cei infectati cu VHC (52%) decat la cei neinfectati (5%) (Haddad J. 1992).
Virusurile limfotropice au potentialul de a genera procesul autoimun. Unele regiuni imunoreactive ale proteinelor La /SSA au secventa similara cu cea a proteinelor EBV, ale HHV6 si HIV-l (Haaheim LR. 1996). Pare posibil ca aceste virusuri sa stimuleze productia de autoanticorpi datorita mimetismului molecular sau a expunerii La /SSA la suprafata celulelor dupa translocatia determinantilor self criptici.
Asocierea imtului mamar cu silicon si prezenta ulterioara a simptomatologiei specifica Sindromului Sjogren a fost sugerata de publicarea unor articole ce sustineau prezenta acestor simptome la jumatate din pacientele operate. Aceasta ipoteza nu a putut fi dovedita. Nu exista o corelatie stiintifica ci doar o baza teoretica limitata pentru aceasta asociere. De asemenea s-a raportat asocierea depozitelor de amilod la nivel mamar la unele paciente diagnosticate cu SS primar (Kersemans R. 2006).
Studiile populationale si familiale au aratat infuenta importanta a factorilor genetici asupra susceptibilitatii la bolile autoimune, de exemplu diabetul zaharat, poliartrita reumatoida, lupusul eritematos sistemic, Sindromul Sjogren, sunt cele mai tipice exemple.
Terenul genetic pe care evolueaza Sindromul Sjogren primar este cel al Ag. HLA B8 / HLA DR3, iar pentru cel secundar este imprumutat cel al bolii cu care se asociaza (HLA DR4- pt poliartrita reumatoida, HLA DR2, DR3, DQ2, DQ6 -pt Lupusul Eritematos Sistemic). Deoarece sunt citate aglomerari familiale ale sindromului se poate discuta de susceptibilitate genetica asupra careia actioneaza factori virali si alti factori de mediu incriminati in etiopatogenia Sindromului Sjogren.
Analizele imunohistologice ale infiltratului limfocitar celular din glandele salivare ale pacientilor cu Sindrom Sjogren (SS) arata o predominanta a limfocitelor T si mai putine celule B si macrofage. Majoritatea limfocitelor T sunt (CD4+) si raportul intre CD4/ CD8 este cu mult peste 2. Multe dintre aceste celule T poarta fenotipul cu memorie CD45 RO+ si exprima receptorul α/ β al celulei T si LFA1 si pot participa semnificativ la hiperactivitatea celulelor B.
Expresia aberanta a moleculelor HLA din epiteliul glandelor salivare
al pacientilor cu SS sugereaza ca aceste celule pot
functiona ca celule prezentatoare de antigen non-profesioniste
interactionand cu celuleleT (CD4+). O astfel de interactiune poate
conduce la productia ulterioara de citokine si la stimularea
proliferarii si diferentierii celulelor B. De exmplu, nivele
inalte de IL1-β, IL6 si TNF-α sunt produse de celulele
epiteliale, in timp ce IFN-γ si IL10 sunt produse in principal de
celulele T infiltrate. De asemenea IL10 si IL6 sunt produse in
cantitati crescute in sangele periferic. Un nivel scazut
neidentificat al IL2 in SS se poate datora absentei semnalelor
co-stimulatoare al
O degradare anormala a unei proteine ce apartine citoscheletului (α-fodrin), a fost demonstrata in glandele salivare a unor soareci experimentali pentru SS, la 3 zile post-timectomie. Aceasta degradare anormala conduce la exprimarea unei proteine de 120 kDa, exclusiv in glandele salivare. Soarecii au dezvoltat atat autoanticorpi cat si imunitate celulara fata de acest antigen (Haneji N.1997). In primul studiu uman, 41 din 43 de pacienti cu SS primar au prezentat anticorpi anti α-fodrin (Witte T.2000). Un singur studiu a analizat sensibilitatea si specificitatea prezentei anticorpilor anti α-fodrin la pacientii cu SS p, iar acestea au fost 70% si 93% (Kuwana M. 2001).
Alti autoanticorpi descoperiti sunt anticorpii anti receptor muscarinic M3 si anticorpi anti ICA 69 (proteina a carei functie nu este cunoscuta si care se exprima la nivelul celulelor β pancreatice, a neuronilor si a glandelor salivare.
Mecanismul complet de distructie glandulara ramane inca neelucidat. Celulele T citotoxice pot juca un rol important in acest sens. Dupa recunoasterea adecvata a complexului antigenic MHC prezentat de o celula tinta, celulele citotoxice induc moartea celulara prin una dintre cele doua cai independente, cea mediata de perforine sau cea mediata Fas. Pe calea din urma semnalul apoptotic este transmis la celula tinta prin crosslinkage a doua molecule de suprafata celulara: FasL al celulei citotoxice si Fas al celulei tinta. Fas face parte din familia receptorilor TNF-α si se exprima constitutiv sau dupa stimularea variatelor celule printre care si celulele epiteliale. Fas L este o proteina transmembranara de tip II exprimata in regiuni non- limfoide, cum ar fi corneea, testiculul si pe limfocitele activate. Expresia Fas a fost descoperita in infiltratul celular mononuclear al glandelor salivare la soareci cu o afectiune similara Lupusului Sistemic Eritematos si SS (Skarstein K 1997). Apoptoza este importanta pentru down-regulation a raspunsului imun dupa activarea si proliferarea celulelor B si T. Expresia defectuoasa a Fas si Fas L poate avea ca si consecinte, acumularea de limfocite mature si poate contribuii la dezvoltarea unei boli autoimune. O cale defectuoasa Fas Fas L a fost de asemenea demonstrata la soarecii cu afectiuni similare SS.
Prin tehnici PCR si analize imunohistochimice din glandele salivare minore au fost puse in evidenta prezenta Fas, Fas L, bcl2, la pacienti cu SS (Nakamura H 1998). Celulele epiteliale ductale si acinare exprima un nivel anormal al Fas si Fas L la pacientii cu SS si mai ales in cazul in care exista un infiltrat mononuclear sever. Celulele epiteliale care exprima Fas sunt situate in apropierea sau in interiorul unui focus. Cele care exprima Fas L sunt in infiltratul celular mononuclear, periacinar sau in jurul ductelor. Aceste descoperiri confirma ipoteza ca Fas L de pe celulele T citotoxice infiltrante este crosslinkat pe Fas al celulelor glandulare inducand apoptoza acestor celule. Studii in situ au aratat un nivel scazut sau chiar absenta apoptozei in randul celulelor din infiltratul mononuclear. Up-regulation a expresiei Bcl 2 a fost detectata ca participant la inhibarea apoptozei acestor celule. Alti factori extrinseci care ar putea bloca apoptoza limfocitelor T sunt citokinele (IL-2, IL-l0, TNF-α) si moleculele de adeziune.
De asemenea si calea perforinelor a limfocitelor T cititoxice participa la patogenia bolii asa cum au aratat o serie de studii.
Leziunile clasice anatomopatologice sunt constituite din infiltrat limfoplasmocitar distribuit in jurul ductelor glandulare intralobulare, atrofie acinara, modificari metaplazice si proliferative ale celulelor ductale, scaderea pana la disparitie a tesutului adipos.
Din punct de vedere morfopatologic glandele salivare sunt cel mai bine studiate datorita afectarii lor frecvente si accesibilitatii exploratorii crescute. Modificarile histologice care se descriu sunt similare la nivelul tuturor tesuturilor exocrine afectate. La fel si in cazul coafectarilor parenchimatoase si chiar a ganglionilor limfatici care capata uneori aspect pseudolimfomatos. Infiltratul inflamator cu limfocite, monocite si plasmocite este localizat initial periductal si difuzeaza centrifug odata cu distructia acinara. In evolutie apare inlocuirea progresiva cu limfocite a epiteliului salivar normal pentru ca, in stadiile tardive sa intalnim zone de fibroza si acini distrusi, infiltrat inflamator cronic precum si elemente ductale care uneori pot fi obstruate sau dilatate. Caracteristica este pastrarea septurilor ductale interlobulare. In ceea ce priveste componenta infiltratului se observa o predominanta a limfocitelor TH(CD4+) fata de cele TH(CD8+), acestea fiind de trei ori mai putine. Limfocitele B, desi reprezinta doar 1/5 din totalitatea infiltratului sunt hiperreactive, fiind responsabile de productia crescuta de anticorpi. Apoptoza celulelor glandulare poate fi considerata ca evenimentul care expune particulele de acizi nucleici sistemului imun ceea ce duce la aparitia acestora (Anticorpi Anti Nucleari, Factor Reumatoid). Exista si autoanticorpi anti-organ specifici, anticorpi anti receptor Muscarinic (M3).
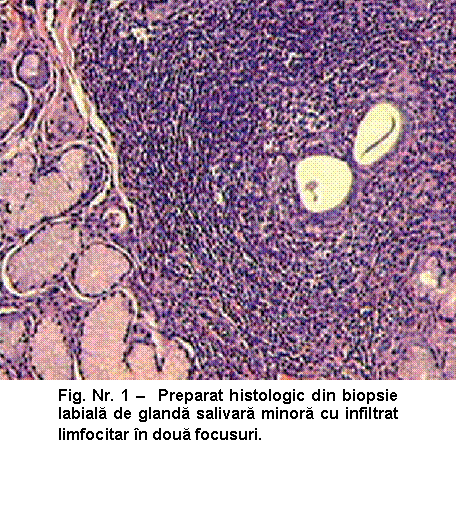
Aspectul histologic descris are o deosebita importanta pentru interpretarea biopsiei de glanda salivara minora. Pot fi vizualizate modificari precoce (infiltrat limfoplasmocitar periacinar) chiar atunci cand celelalte probe efectuate pentru obiectivarea scaderii secretiei salivare sunt negative.
S-a demonstrat cA ingestia repetatA a unor cantitAti de alcool in cursul primelor luni de sarcinA duce la aparitia unor trAsAturi dis-morflce si [...] |
Se defineste prin: 1) evacuari intestinale la intervale mai mari de 48 de ore; 2) scaune de consistenta crescuta; 3) evacuari incomplete, A [...] |
Sindromul hipoton se caracterizeaza prin diminuarea, de obicei marcata, a tonusului si a activitatii musculare spontane si voluntare, realizand [...] |
Copyright © 2010 - 2025
: eSanatos.com - Reproducerea, chiar si partiala, a materialelor de pe acest site este interzisa!
Informatiile medicale au scop informativ si educational. Ele nu pot inlocui consultul medicului si nici diagnosticul stabilit in urma investigatiilor si analizelor medicale la un medic specialist.
Termeni si conditii - Confidentialitatea datelor - Contact