|
|
DIAGNOSTICUL TUMORILOR TESTICULARE
Diagnostic clinic
Supozitia clinica de cancer testicular ramane cheia de bolta a diagnosticului pozitiv precoce de tumora testiculara, examenul clinic atent ramanand cea mai buna metoda de diagnostic. TTG reprezinta o problema de sanatate publica. Desi incidenta lor este de 1-2% din totalul neoplaziilor, ele reprezinta prima cauza de cancer la adultul tanar intre 15-35 de ani. Aceasta perioada de viata reprezinta cea mai importanta etapa de afirmare pe social si profesional54. In plus, asa cum am amintit anterior, datele epidemiologice atesta o crestere a incidentei TTG in toate tarile de rasa alba, cu o tendinta de a egala incidenta limfoamelor maligne la sexul masculin. Astfel, Skinner D. raporteaza o crestere a neoplaziei de 2-3 ori in zona Los Angeles-ului, iar seriile Dateca din Danemarca arata o crestere a incidentei de 1,5 ori in ultimii 10 ani54. Consecutiv progresului remarcabil in managementul acestei neoplazii, datorat perfectionarii tehno-logiei de stadiere (CAT, markeri tumorali) si chimioterapiei specifice inalt eficiente care au transformat cancerul testicular intr-un model de neoplasm solid curabil57, majoritatea pacientilor (din pacate nu toti) pot fi salvati, in ciuda unui lung interval de timp de la debutul aparent clinic la diagnostic, deci in stadii avansate de boala. Ponderea stadiilor diseminate la momentul primului diagnostic este estimata la 1/3 cazuri Donohue J.P.15, Richie J.55 2/3 cazuri Proca E.54 Aceasta inseamna cost social si medical crescut, chimioterapie de durata si chirurgie extensiva, deci morbiditate post-terapeutica ridicata.
Toate aceste consideratii justifica elaborarea unui test de screening pentru can-cerul testicular germinal adresat populatiei masculine cu risc, diagnosticul bolii in stadiile preinvaziv si clinic initial permitand scurtarea intervalului de boala, un trata-ment mai putin agresiv si costisitor, precum si reducerea consecintelor neplacute ale bolii57.
Examenul clinic efectuat de catre un examinator cu experienta ramane in con-tinuare principalul test de screening72. Alterntiva ecografiei testiculare (mult mai sensi-bila) doar ca test screening nu este benefica sub raport cost-eficienta42.
Screening-ul clinic este recomandat de Societatea Americana pentru Oncologie Clinica si Institutul National pentru Cancer din SUA pentru a fi inclus obligatoriu in examenul periodic de sanatate la barbati42.
Pe de alta parte, raritatea cancerului testicular si limitele sensibilitatii screening-ului clinic (examenul fizic al scrotului de catre clinician) fac ca practicarea examenului de rutina la toti barbatii asimptomatici, desi ieftina, sa aiba un randament redus. Astfel, grupurile de studiu nord-americane The Canadian Task Force and The US Preventive Service Task Force42 recomanda examinarea fizica atenta a testiculului ca test screening, dar limitat la categoriile de barbati cu factori de risc in antecedente (criptorhidie, TTG in antecedente, istoric familial).
Depistarea precoce a cazurilor simptomatice reprezinta o tentativa similara, fiind adresata pacientilor cu semne clinice de alarma : nodul testicular-masa scrotala, cu/ fara durere locala, cu/ fara fenomene inflamatorii asociate. Clinicianul53 trebuie sa aplice vechiul, dar mereu actualul principiu conform caruia orice tumora descoperita la nivelul testiculului este cancer pana la proba contrarie. Reducerea mortalitatii prin cancer testicular presupune surprinderea bolii intr-un stadiu localizat.
Importanta prognostica a acestui deziderat este evidentiata de relatia dintre intervalul diagnostic (durata de timp scurs intre debutul aparent clinic si momentul diagnostic, respectiv al terapiei specifice) si rezultatul terapeutic.
Astfel, Oliver si colab. 42 constata un timp mediu de amanare a diagnosticului de doua luni la cei vindecati, de patru luni la cei cu recidiva a bolii, dar care sunt controlati terapeutic si de sapte luni la cei care decedeza. Desi chimioterapia actuala de linia a doua si de salvare poate asigura raspuns clinic complet si la pacientii cu forme avansate de boala, prelungirea intervalului diagnostic este in continuare responsabila de mortalitate prin TTG. Descresterea acestui interval reprezinta un deziderat major, fiind o eficienta metoda de ameliorare a supravietuirii prin cancer testicular si de reducere a costului, respectiv morbiditatii secundare tratamentului. Studii multicentrice au precizat o durata medie de cinci luni a acestui interval diagnostic42.
Relevanta prognostica a acestui criteriu clinic difera in functie de natura histo-logica a TTG. Astfel, TGS pure, care reprezinta aproape jumatate din cazurile de TTG, au un lung interval de evolutie locala, iar prezenta determinarilor secundare la distanta inregistreaza un raspuns terapeutic foarte bun la chimioterapie, supravietuirea nefiind afectata semnificativ, liniar de acest interval. TGNS, biologic diferite de cele semino-matoase, prezinta o crestere mai rapida, devenind invazive precoce, dupa o perioada preclinica foarte scurta.
In cazul TGNS, amanarea momentului diagnostic are repercusiuni prognostice profund defavorabile, fiind responsabila de o evidenta crestere a mortalitatii. TGNS sunt prototipul biologic al tumorilor germinale cu evolutie rapida, fara o perioada de evolutie preclinica decelabila.
Factorii ce tin de pacient cuprind: lipsa de educatie sanitara, ignoranta, frica de cancer si de castrare. Spre deosebire de alte categorii de cancere, pacientii cu tumori testiculare sunt mai inclinati sa refuze sau amane gestul terapeutic primar orhidecto-mia datorita impactului psihic al pierderii unui organ sexual la o varsta la care sexua-litatea are un rol major in viata psihosociala (body-image). Indiscutabil ca acest aspect imbraca conotatii culturale si religioase mai ample si, nu ne miram, reamintindu-ne reactia varstnicului cu cancer prostatic care refuza castrarea.
Rolul erorii medicului curant se datoreaza lipsei de experienta, examenului fizic incomplet si formelor clinice inselatoare. Cruciala ramane recomandarea de a ne gandi la cancerul testicular in orice suferinta scrotala, urmand a ne adapta demersul diagnostic si terapeutic in mod dinamic.
Forma clinica franc tumorala, asociind durerea locala si ascensiunea termica prin hemoragie intratumorala, continua sa preteze la confuzia cu orhiepididimita acuta in 30% din cazuri, fiind responsabila de o intarziere diagnostica in medie cu doua-trei luni. Proca E. afirma in acest sens53: Am facut-o poate si noi, si probabil o vom mai face, dar am limitat proba clinica (antibioterapia) la doua-trei saptamani si am efectuat totdea-una ecografie testiculara in acest interval pentru a exclude tumora primara. Consideram condamnabila nu atat eroarea diagnostica initiala, cat obstinatia de a trata o leziune infectioasa inflamatorie acuta luni de zile, iar forma nodulara, mimand epididimita cronica, chiar ani de zile!
In experienta noastra (o serie de 201 cazuri consecutive de TTG9), am consemnat tratamente antibiotice pentru presupuse orhiepididimite acute in 26% din cazuri. Absolut condamnabil, in unele cazuri, antibioterapia s-a extins pe perioade de timp incompatibile cu caracterul presupus acut al bolii de baza (sase luni in 2 cazuri; un an in 2 cazuri; peste 2 ani in 2 cazuri !).
Simptomatologia stadiilor metastatice (masa tumorala abdominala, adenopatiile periferice, durerile abdominale, hemoptizia, fracturile, etc.) realizeaza, asa cum am vazut, sindroame polimorfe, ce pot preta la confuzie si intarziere diagnostica, a caror cauza majora o reprezinta lipsa de examinare a scrotului.
Efortul de a reduce intervalul de timp pana la diagnostic presupune un ansamblu de masuri organizatorice (subprogram oncologic national) tintind atat pacientii, cat si reteaua medicala, in scopul cresterii gradului de sensibilizare, public si medical, in fata neoplaziei:
informarea populatiei masculine despre semnele si simptomele de debut ale bolii (brosuri de popularizare a riscului de cancer testicular, a semnelor de alarma: tumora, durere, senzatie de testicul greu);
informarea medicilor de prim contact, cu criteriile de risc crescut pentru TTG si semnele clinice ale bolii;
obligativitatea examenului fizic complet, inclusiv a regiunii genitale externe cu prilejul oricarui consult medical si, in orice caz, cu prilejul controalelor medicale obligatorii (la recrutare, la angajare, control periodic general anual in cadrul asigurarii de sanatate);
obligativitatea explorarii ecografice a suferintelor scrotale si a limitarii antibio-terapiei pe criterii clinice a orhiepididimitelor acute la 2-3 saptamani, esecul terapeutic deferind pacientul specialistului urolog;
abtinerea de la manevre diagnostice peiorative oncologic (punctia biopsie) si explorarea corecta a testiculului patologic (care trebuie facuta pe cale inghinala, cu clamparea funiculului spermatic la orificiul inghinal profund in caz de dubiu diagnostic) in reteaua de chirurgie.
Nu in ultimul rand, similar programului de screening pentru cancer mamar, s-a recomandat autopalparea testiculara ca metoda de diagnostic precoce. Societatea Americana pentru Cancer si Institutul National de Cancer din SUA au recomandat acest examen pentru toti barbatii de varsta postpubertara, cu o ritmicitate lunara .
Educarea populatiei masculine in sensul acestui autocontrol corect este inca controversata, nu toti specialistii considerand-o benefica (US Preventive Services Task Force). Altii o recomanda numai barbatilor cu factori de risc crescut (Moul J.W., 199842). Caracterul ei anodin ne face insa sa o sustinem fara rezerve. Tehnica autoexaminarii presupune:
familiarizarea pacientului cu anatomia, consistenta si suprafata normala a propriului testicul
efectuarea autopalparii cu prilejul baii sau dusului (cu apa calda)
identificarea corecta a epididimului pentru a-l diferentia de o tumora
rularea testiculului intre index si police pentru palparea atenta a ambelor testicule
comunicarea imediata medicului a oricarei modificari de suprafata sau consistenta a glandei.
Examenul clinic al continutului scrotal52 incepe prin inspectia sacului scrotal, aspectul acestuia putand fi normal sau destins si deplisat de partea afectata datorita dimensiunilor tumorii (.13.a).
Palparea continutului scrotal se va face bimanual, cu blandete, incepand cu bursa controlaterala, ceea ce va permite aprecierea ativa a marimii, formei, suprafetei si consistentei testiculului normal, apoi a celui patologic. Testiculul normal este usor sensibil, mobil si perfect delimitabil de epididim prin prezenta santului interepididimo-testicular (clasicul semn al lui Chevassu), avand o forma ovoidala si consistenta omo-gena, scazuta. Identificarea epididimului constituie manevra esentiala a examenului lo-cal, acest lucru facandu-se prin prinderea sa intre policele si indexul mainii examina-toare, degetele rulandu-l apoi cranial si caudal de-a lungul santului interepididimo-testi-cular, pentru a-i delimita capul si coada.
Orice zona de consistenta inegala in interiorul tunicii albuginee trebuie sa atraga atentia. In fazele locale franc tumorale, palparea va releva prezenta unei induratii (nodul tumoral) cu Ø pana la cativa centimetri, nedureroasa, ce deformeaza ovoidul glandei. Extensia la epididim, funiculul spermatic si tegumentul scrotal survine in fazele locale avansate. Evolutia locala indelungata este particulara seminoamelor si teratoamelor mature, realizand o marire globala a glandei, cu respectarea formei ovoidale a acesteia (seminom), dar cu consistenta dura si suprafata neregulata (teratom).
In 10% din cazuri poate coexista un hidrocel secundar, ceea ce reduce sensibilitatea palparii pana la a o anula, impunand explorarea ecografica a actorului de dupa cortina15, 54.
In rezumatul submodulului dedicat diagnosticului clinic, consideram util a sublinia rolul diagnostic al:
decelarii anamnestice a
o varstei de risc (20-34 ani)
o principalilor factori de risc (testicul necoborat sau coborat chirurgical, cancer testicular controlateral in antecedente; cancer testicular in familie)
o vechimii si cronologiei semnelor si simptomelor locale de boala
o existentei, in istoricul masei tumorale scrotale sau inghinale, a unor gesturi chirurgicale ofensatoare oncologic (punctii bioptice, cura herniei sau hidrocelului satelit, explorari chirurgicale nefinalizate ablativ, ablatia pe cale scrotala a testiculului tumoral)
examenului clinic al bursei scrotale (palparea bimanuala a glandei, cu blan-dete, cu pensarea vaginalei si identificarea palpatorie a epididimului si funiculului spermatic, precum si evaluarea mobilitatii invelisurilor scrotale fata de masa tumorala; decelarea unei burse scrotale goale, in contextul existentei unei tumori pelviabdominale)
examenului clinic al grupelor adenopatice periferice (inghinale, axilare, supra-claviculare)
examenului clinic al abdomenului pentru decelarea palpatorie a tumorii (testicul necoborat, tumoral) sau a maselor adenopatice retroperitoneale
examenului clinic toracopulmonar (ginecomastie, sputa hemoptoica, semne de revarsat pleural).
Din prezentarea exhaustiva a complexului tablou clinic al TTG rezulta ca, marea majoritate a tumorilor, se dezvolta pe testicul coborat normal sau chirurgical in bursa scrotala deci usor accesibil clinicianului precum si faptul ca, in aceeasi masura, debutul aparent clinic cuprinde semne si simptome locale.
Datele prezentate constituie argumente convingatoare pentru asertiunea conform careia examenul clinic minutios ramine fundamental in diagnosticul pozitiv de cancer testicular, chiar si in contextul actual al tehnologiei imagistice si bioumorale perfor-mante. Acest examen va sugera existenta cancerului testicular, urmand ca investigatiile paraclinice sa o confirme, iar examenul histopatologic al piesei operatorii sa certifice prezumptia clinica.
Investigatiile paraclinice vor confirma prezumptia clinica de tumora testiculara si vor stabili amploarea extensiei acesteia la distanta, definind diagnosticul stadial clinic preterapeutic.
Protocolul standard de diagnostic clinic al unei tumori testiculare include (Societatea Romana de Urologie 51, Societatea Romana de Chirurgie Oncologica 65) obligatoriu, pe langa examenul clinic local si general al pacientului:
1. ecografia testiculara (scrotala/ inghinala/ abdominala)
2. radiografia toracica standard
3. tomografia computerizata abdominopelvina
4. markerii tumorali (AFP, b-HCG, LDH seric, GUT)
5. examenul anatomopatologic al piesei de orhidectomie.
Optional sunt utilizate urografia, limfografia bipedala, scintigrafia (hepatica, osoasa, cerebrala), ultrasonografia retroperitoneului, rezonanta magnetica nucleara, markeri tumorali citogenetici sau imunohistochimici, anatomia patologica a elementului stadial N/M (material patologic recoltat operator) .
Bilantul preterapeutic standard va include obligatoriu o evaluare bioumorala (hemograma, teste de functie renala si hepatica in special) si cardio-pulmonara avand in vedere efectele toxice ale terapiei adjuvante. Considerand varsta tanara a pacientilor, precum si riscul teratogen al terapiei adjuvante specifice, unele centre de excelenta in cancer testicular din sisteme de sanatate vestice includ recoltarea preterapeutica de sperma de la pacienti pentru o posibila fertilizare ulteriora in vitro, avand in vedere potentialul semnificativ de curabilitate al neoplaziei chiar in stadii diseminate.
Diagnostic imagistic
Ecografia
Diagnosticul pozitiv de tumora testiculara, prezumat clinic, trebuie obligatoriu confirmat prin ecografie scrotala cu transducer de 8 MHz (Richie J.P. 55). Aceasta va preciza caracterul solid sau hipoecogen al leziunii (.5.), dimensiunea nodulului tumoral, structura omogena sau neomogena a acestuia si va aprecia gradul invaziei locale prin interesarea anexelor. Ecografia se va adresa regiunii canalului inghinal, pentru testiculul aflat in ectopie inghinala sau abdomenului, pentru testiculul criptorhid.
Ecografia scrotala a ajuns practic o extensie a examenului clinic. Repetabilitatea, inocuitatea si performantele de acuratete la care s-a ajuns au impus-o in evaluarea diagnostica a leziunii primare. Specificitatea si sensibilitatea deosebite la care s-a ajuns datorita utilizarii unor sonotrozi de 8 si 10 MHz in regim real-time cu rezolutie mare o impun in protocolul de diagnostic pozitiv al tumorilor testiculare. Utilizarea ecografiei in caz de dubiu diagnostic poate scurta clasicul tratament de proba in cazul maselor scrotale cu alura clinica de orhiepididimita (2-3 saptamani).
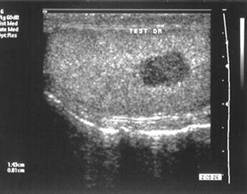 .5. Nodul
hipoecogen testicular drept
.5. Nodul
hipoecogen testicular drept
(cazuistica Clinicii Fundeni)
Sonografia poate distinge net nodulul tumoral intratesticular de epididimul in-flamat sau formatiuni tumorale paratesticulare, permitand explorarea glandei si dincolo de cortina reprezentata de hidrocelul adeseori asociat10,55. Astfel, Sample si colaboratorii gasesc o sensibilitate de 80% a metodei pe un lot de 55 tumori testiculare operate, iar Richie constata pe un lot de 22 de cazuri doar trei rezultate fals negative si nici un rezultat fals pozitiv.
Metoda poate detecta leziuni solide cu diametrul de 5 mm, dar, fiind o explorare morfologica, nu va putea distinge tipul histologic al TTG.
Studii recente arata o specificitate de 95% si sensibilitate de 100% pentru eco-grafia testiculara cu sonotrozi de 8 si 10 MHz, conferind metodei o valoare deosebita, nu doar in explorarea testiculului patologic, ci si in supravegherea activa a celui congener (depistarea CIS).
Valoarea informativa a ultrasonografiei in explorarea spatiului retroperitoneal este mai redusa datorita excesului de tesut adipos si continutului hidroaeric al masei intestinale3, 42. Sensibilitatea metodei creste pentru masa adenopatica voluminoasa N2 si N3 (bulky disease). Aspectul sonolucent, aproape chistic, cu contur policiclic, in strans contact cu aorta sau vena cava inferioara defineste prezenta adenopatiilor retroperito-neale.
Principalul handicap al metodei este deci ignorarea stadiilor de invazie retro-peritoneala minima, ceea ce confera ecografiei retroperitoneale un rol secundar, optional in cadrul protocolului de stadiere al TTG, testul neavand valoare predictiva in caz de rezultat negativ (N0).
Radiografia toracica standard
Va preciza existenta interesarii toracopulmonare35, cunoscut fiind faptul ca mediastinul si plamanul ocupa locul al doilea in ordinea metastazarii dupa limfaticele retroperitoneale. Imaginea tipica54 a metastazei pulmonare o reprezinta clasicul aspect al tevii de lansat baloane, unde balonul este metastaza, iar teava limfangita neoplazica (. 6.a.). Sensibilitatea ei este de 85-90%37. Comparativ, radiografia toracica standard deceleaza noduli cu diametrul de 1 cm, radiotomografia leziuni de 5-6 mm, iar tomo-grafia computerizata noduli de 3 mm (acest spor de sensibilitate se insoteste insa de o scadere a specificitatii examenului TC prin detectia de leziuni granulomatoase benigne).
Largirea siluetei mediastinale prin adenopatie metastatica (. 6.b.) la acest nivel reprezinta alt semn radiologic toracic definitor al bolii in stadiul supradiafragmatic52.
a) 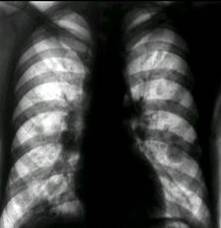 b)
b) 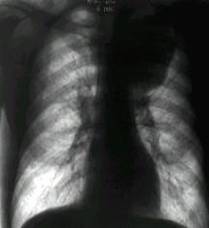
. 6. Semne radiologice toracice de boala diseminata stadiu III (cazuistica Clinicii Fundeni)
Radiografia toracica standard va fi efectuata de rutina42, examenul CAT toracic urmand a fi efectuat doar in cazuri selectionate, dupa examenul CAT abdominal. Riscul predictibil de metastazare pulmonara in N2 si N3 va dicta (cost-eficient) oportunitatea CAT toracica35.
Un interesant studiu publicat de See si Hoxie, 1993 63 de la Departamentul de Urologie al Universitatii Jowa analizeaza ativ valoare informativa a radiografiei toracice standard si a CAT toracice ca modalitati de stadiere imagistica la pacientii cu TTG in functie de rezultatul stadierii CAT abdominala (N0/N+). Considerand caracterul secvential predictibil al metastazarii TTG, rezulta ca pacientii cu CAT abdominal negativ au un risc scazut de metastazare toraco-pulmonara (low risc), spre deosebire de cei high risc, cu CAT abdominal pozitiv. CAT abdominal reprezinta un factor predictiv valoros cu privire la riscul metastazarii toracice; doar 4% din pacientii CAT abdominal negativi au avut Mpl la prezentare, fata de 40% din cei CAT abdominal pozitivi. Vom prefera stadierea toracica a TTG prin radiografie toracica standard la pacientii fara invazie ganglionara retroperitoneala (N0) la evaluarea CAT abdominala; pacientii depistati cu invazie ganglionara la CAT abdominala sunt candidati la CAT toracica in cazul unei anomalii radiologice.
Tomografia computerizata abdominopelvina
Reprezinta, indiscutabil, achizitia imagistica radiologica cea mai importanta in protocolul de stadiere a tumorilor testiculare38. Este metoda de electie pentru explorarea spatiului retroperitoneal, respectiv a ganglionilor periaortici si pericavi (prima statie de diseminare a tumorii testiculare), putand decela ganglioni mici cu Ø pana la 5 mm, nedecelati de ecografie, limfografie, cavo si urografie. Sensibilitatea metodei atinge 80%, fiind invers proportionala cu stadiul. Specificitatea este apreciata diferit de diversi autori (83-l00%)38, 56. La acestea se adauga agresivitatea redusa, ativ cu celelalte metode radiologice de explorare a teritoriilor limfatice retroperitoneale.
Perfectionarea rezolutiei la aparatele de generatie recenta a redus limita de detectie a adenopatiei de la 1,5 la 0,5 cm Ø, ceea ce, combinat cu studiul markerilor tumorali si elaborarea unor scheme citostatice foarte eficiente, a permis temporizarea limfadenectomiei retroperitoneale in stadiile I, IIA si IIB de boala. Aceasta crestere a sensibilitatii in diagnosticul CAT se face insa in detrimentul specificitatii, informatia tomodensimetrica neputand discrimina intre leziunile benigne si maligne la Ø sub 1 cm .
Handicapul metodei este dat de faptul ca dimensiunea ganglionara reprezinta singurul criteriu de anormalitate (invazia tumorala metastatica neputand fi detectata) si de costul ei ridicat. In plus, valoarea predictiva a rezultatelor fals negative (N0 ) este de doar 56% (Richie).
Valoarea CAT abdominale in stadierea retroperitoneala ar trebui sa rezide nu doar in capacitatea ei de a depista invazia ganglionar-limfatica, ci si in increderea acordata unui examen negativ, adica in valoarea predictiva a unui rezultat negativ (N0), mai ales daca se are in vedere solutia wait and see fata de limfadenectomia retroperitoneala de stadiere.
Astfel, studiind un lot de 30 de pacienti cu toate stadiile de boala explorat prin CAT abdominala in saptamana premergatoare limfadenectomiei retroperitoneale, Richie constata o sensibilitate a metodei de 65%. Din 16 examene N0, 7 au fost fals negative (44 %), rezultand o valoare predictiva a rezultatelor negative N0 de 56 % in aceasta serie. Rata crescuta a rezultatelor fals negative este confirmata si de alte centre (Sloan Kettering si Universitatea Indiana).
Analizand un esantion de 24 pacienti stadiati CAT (15 stadii I, 9 stadii II ) si supusi limfadenectomiei retroperitoneale primare de stadiere, am9 constatat 6 erori de stadiere CAT: 3 subestimari (real N+ ; LARP primara pozitiva in stadiu I CAT) si 3 supraestimari (real N0; LARP primara negativa in stadiul II CAT). Astfel, valoarea predictiva a CAT abdominopelvine in seria Clinicii urologice Fundeni (1982-l993) a putut fi apreciata la 83% pentru testul negativ, respectiv 75% pentru testul pozitiv.
a) 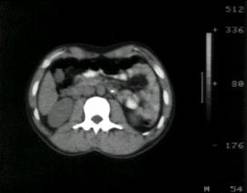 b)
b) 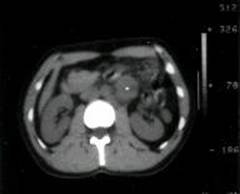
. 7. CAT abdominala in boala adenopatica retroperitoneala N2 (a), N3 (b) (cazuistica Clinicii Fundeni)
Capacitatea metodei de a decela boala adenopatica minora, adenopatia mediastinala de mici dimensiuni, metastazele pulmonare, hepatice, osoase fac din examenul TC metoda de electie pentru stadierea cancerelor testiculare.
Tomografia computerizata abdominopelvina si, la nevoie toracica, reprezinta un excelent mijloc neinvaziv de urmarire a rezultatului terapeutic si control stadial. Limita informatiei intervine in situatia in care masa adenopatica, care a scazut initial sub tra-tamentul citostatic, devine stagnanta. In acest caz, unica modalitate de stadiere corecta este reprezentata de examenul histopatologic al materialului recoltat prin limfade-nectomie retroperitoneala secundara13.
Celelalte metode imagistice adresate spatiului retroperitoneal nu ofera informatii superioare examenului TC, fiind facultative la ora actuala. Lista acestora include:
Examenul in rezonanta magnetica nucleara
Este mai scump; nu s-a dovedit superior tomografiei computerizate in diagnosticul adenopatiei retroperitoneale la ora actuala42.
Avantajele metodei ar consta in posibilitatea de a obtine imagini in uri multiple ale adenopatiilor, precum si in capacitatea de a aprecia marimea ganglionilor fara utilizarea substantei de contrast si fara riscul de iradiere5. Posibilitatea de a efectua sectiuni sagitale la pacientii cu mase tumorale adenopatice voluminoase, ofera o de-limitare mai precisa a limitelor superioare si inferioare fata de examenul CAT, precum si precizarea aderentei tumorii la structuri vasculare foarte importante pentru chirurg (aorta, cava abdominala, pediculul renal, vasele iliace primitive).
Limfografia bipedala
Are o valoare istorica54,55, fiind utila in decelarea adenopatiilor retroperitoneale cu o acuratete globala estimata la 62-89%. Se obtine prin injectarea de substanta de contrast in vasele limfatice de pe fata dorsala a ambelor picioare sau intr-un vas limfatic din funiculul spermatic descoperit cu ocazia orhidectomiei inghinale si efectuarea de radiografii abdominale si toracice seriate in urmatoarele 24 de ore54. Rata mare a rezultatelor fals pozitive si negative (valoare predictiva fals negativa de 26%), caracterul agresiv (complicatiile postmanevra cuprind stari febrile, durere locala, infectia plagii si disfunctia respiratorie severa) precum si existenta, la ora actuala, a unor metode mult mai sensibile si mai putin agresive (CAT si ecografia) au scos-o din protocolul investigational obligatoriu de stadiere. Limfografia permite, in faza de umplere limfatica, vizualizarea de imagini de oprire a substantei de contrast sau staza la nivelul trunchiurilor limfatice, iar in faza ganglionara de lacune sau absente ale opacifierii unui grup ganglionar, eventuala crestere de volum si neregularitatea unuia sau mai multor ganglioni52. Limfografia permite deasemenea ghidarea chirurgiei limfatice retroperitoneale si a radioterapiei. Unii autori apreciaza ca 20-30% din metastaze sunt oculte, cu examen tomografic si limfografie normale.
Urografia intravenoasa
Ofera semne tardive52,54: laterodevieri ureterale, diverse grade de ureterohidro-nefroza prin compresie adenopatica extrinseca, mergand pana la mutism renal. Desi fa-cila in executie si rutiniera intr-un serviciu de urologie, metoda are o sensibilitate redusa, apartinand etapelor evolutive tardive ale stadiului de boala retroperitoneala (N2, N3).
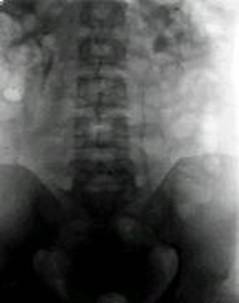
. 8. U.I.V. Laterodeviere
ureterala drapta prin compresiune adenopatica extrinseca
(cazuistica Clinicii Fundeni).
Flebografia venei cave inferioare
Se executata prin cateterism percutanat femuroiliac54; nu furnizeaza informatii in stadiile initiale de boala retroperitoneala. Semnele flebografice (impingerea, compresia extrinseca a venei cave; obstructia intrinseca partiala sau totala prin tromboza neopla-zica) reprezinta informatii tardive, specifice stadiilor avansate de boala adenopatica abdominala IIC si III, asa numitele bulky abdominal disease.
Dezavantajul invazivitatii, cu tot cortegiul de posibile complicatii ale punctiei si cateterismului venos, este practic anulat de posibilitatea moderna a efectuarii flebo-grafiei cavei abdominale in cadrul angiografiei digitalizate, dar valoarea informativa ramane aceeasi, limitata in plus de accesul la tehnologie si costul explorarii.
Radiografiile osoase (craniu, coloana lombara, torace fata si profil, bazin osos, oase lungi)
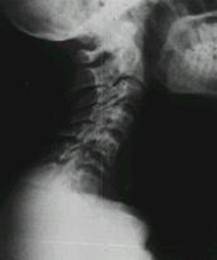
Pot furniza informatii cu privire la metastazele osoase: semne radiografice de osteoliza metastatica52. Examenul radiologic are o sensibilitate mai mica fata de explorarea izotopica (semnele scintigrafice premerg cu 6-l2 luni aparitia semnelor radiologice).
. 9. Tasare de corp
vertebral C7 prin osteoliza metastatica (carcinom embrionar
cazuistica Clinicii Fundeni)
Explorarile izotopice
Cuprind52 scintigrafia osoasa, hepatica, cerebrala si se adreseaza depistarii metas-tazelor. Au avantajul ca nu necesita o pregatire speciala a pacientului, administrarea intravenoasa a radiotrasorului furnizand, in cateva ore, detalii privind amploarea si topo-grafia leziunilor hipocaptante sugestive diagnostic. Vom remarca insa specificitatea redusa a informatiei, existand o serie de afectiuni benigne ce determina lacune de cap-tare, mistificabile ca metastaze riscand suprastadierea (mai ales cele osoase). Efectuarea protocolar obligatorie a CAT abdominale si a radiografiei toracice (ce evalueaza practic complet sediile predilecte de diseminare) confera un rol secundar explorarilor izotopice, limitat la situatiile cand markerii tumorali crescuti coexista cu absenta evidentelor radiologice de determinari tumorale la distanta (exemplul metastazei cu sediu intr-un sanctuar cum este sistemul nervos central). O interesanta utilizare o reprezinta radio-imunodetectia depozitelor tumorale secundare in TGNS prin scanarea corpului pacien-tului dupa administrarea intravenoasa de anticorpi marcati anti -HCG (Javadpour N., 1981) 32.
Markeri tumorali
Markerii tumorali sunt substante proteice care, prin faptul ca sunt secretate in exces de tesutul tumoral germinal, devin indicatori ai prezentei acestuia, uneori cu specificitate de tip histologic42. Conceptul de marker tumoral in clinica umana este intr-un fel legat de TTG, intrucat a debutat prin determinarea prezentei gonadotrofinei corionice umane in urina femeii cu choriocarcinom placentar (Zondek, 1930)42.
Markerii au o valoare deosebita, atat diagnostica (pozitiv si stadial) si prognostica, dar mai ales in urmarirea raspunsului terapeutic54.
Cei mai fiabili si utilizati in practica sunt AFP si HCG, cu toate ca nu sunt markerii ideali (20% din TTG seminoame, teratoame mature nu produc acesti markeri; nici unul din acesti markeri nu este absolut specific TTG). Se folosesc tehnici scumpe de radioimunodozare cu anticorpi specifici. Valorile crescute ale markerilor arata o specificitate maxima si sensibilitate variind in functie de pattern-ului histologic si gradul extensiei metastatice42, 54.
Conceptul de marker tumoral s-a largit in ultimii ani prin adoptarea tehnicilor de imunohistochimie pentru identificarea sintezei de markeri tumorali pe sectiunile de tesut tumoral, cu analiza citogenetica a anomaliilor cromozomiale in celulele tumorale (markeri citogenetici) si gasirea de noi substante cu semnificatie biologica, precum pro-teinele sintetizate de oncogene (markeri moleculari)42.
Unii markeri raman deocamdata de interes experimental: antigenul carcinoem-brionar, antigenul B5 si neuron-specific enolaza (NSE).
Alfafetoproteina este o a1 globulina cu o greutate moleculara de 63-70 kDa, reprezentand proteina serica dominanta in serul fetal la mamifere42. Dupa primul an de viata scade la valori nesemnificative. Nivelul seric normal este sub 20 ng/ml, avand un timp de injumatatire de 5-7 zile. A fost descrisa initial in carcinomul hepatocelular. Creste de asemenea in neoplaziile stomacului, pancreasului, plamanului, precum si in afectiuni nemaligne: citolizele hepatice, hipotiroidie, ataxie telangiectazica. In cancerele testiculare este secretata de elementele sinusului endodermic din tumora42, 54.
AFP serica are un nivel crescut in carcinoamele embrionare (in 70% dintre cazuri) si in tumorile sacului vitelin (75 %), fiind normala in choriocarcinoame, teratoame si seminoame pure (Javadpour N.). Practic deci, valorile crescute ale AFP serice atesta prezenta unui contingent de celule germinale nonseminomatoase in tumora primara; valoarea prognostica a AFP este semnificativa (nivelul lor seric pare invers proportional cu raspunsul la tratament si supravietuirea).
Gonadotrofina corionica umana (HCG) este o glicoproteina de 38 kD, compusa din doua lanturi polipeptidice: a si b54. Subunitatea a este comuna hormonilor hipo-fizari LH, FSH si TSH. Subunitatea b confera specificitate imunologica, este in prin-cipal responsabila de activitatea biologica a tumorilor germinale, fiind specifica pentru gonadotrofina corionica umana.
HCG este secretata de celulele sincitiotrofoblastice placentare (Mostofi, 1984). Cresteri ale b-HCG pot surveni si in alte neoplazii: ficat, stomac, pancreas, plaman, san, rinichi si ca urinara.
Tabel 2.
Originea
celulara a AFP si HCG determinata prin testul imuno-peroxidazei
(preluat din Javadpour N. Sertoli cell tumors of the testis, in Current urologic therapy, Kaufmann J.J.(ed.), Saunders
Comp., 1986 39)
|
TIP CELULAR |
HCG |
AFP |
|
Seminom Seminom cu CGST Carcinom embrionar Carcinom embrionar cu CGST Tumora de sac vitelin cu CGST Choriocarcinom Teratom (matur) |
|
|
* Celule gigante sincitiotrofoblastice
Valorile serice normale sunt sub 1 ng/ml (respectiv 5 mUI/l), avand un timp de injumatatire de 24-36 de ore (45 minute pentru unitatea b)42. Unitatea beta este prezenta in cantitati nesemnificative la barbat, markerul avand o specificitate diferita in functie de tipul tumorii germinale; astfel b-HCG este crescuta la 100% din choriocarcinoame, 60% din carcinoamele embrionare, 25% din tumorile sacului vitelin si sub 10% din seminoamele pure.
Inca nu este precizata semnificatia prognostica a seminoamelor cu productie crescuta de HCG38. Histologic se evidentiaza uneori seminoame cu celule cu aspect asemanator sincitiotrofoblastului, dar distinctia de forma mixta histologic de seminom / teratocarcinom este dificila. Dupa studii recente, pacientii cu seminome asociind valori crescute ale b-HCG ar avea o evolutie nefavorabila la stadii egale de boala. Practic, vom retine ca seminomele pot asocia, intr-un mic procent, cresteri ale HCG, dar acestea sunt modeste. Cresterile mari traduc, categoric, prezenta de elemente germinale nonsemino-matoase in determinarile tumorale secundare54.
Specificitatea globala a ambelor teste este maxima (nu sunt rezultate fals po-zitive). Sensibilitatea pe ansamblul tumorilor testiculare a inregistrat 75% pentru AFP si 51% pentru b HCG, ea crescand odata cu stadiul de boala.
Costul lor ridicat le indica mai putin ca test diagonostic de screening, cat mai ales in urmarirea raspunsului terapeutic, caci valorile crescute dupa tratament indica boala reziduala sau recurenta, impunand masuri terapeutice foarte agresive.
Normalitatea testelor nu indica obligatoriu disparitia completa a tumorii viabile. Astfel, Skinner si Scardino 64 gasesc tumora viabila la limfodisectia retroperitoneala la 80% din pacientii cu markeri normalizati dupa chimioterapie. Similar, Donohue 13.16 gaseste cancer rezidual cu markeri negativi la limfadenectomia retroperitoneala dupa chimioterapia specifica.
Aceasta constatare invita la precautie atunci cand valorile aparent normale ale markerilor pun in discutie decizia de a efectua limfadenectomia retroperitoneala de stadiere.
Dozarile acestor markeri sunt efectuate preterapeutic (valoare starter) si seriat intra si post-terapeutic. Aportul diagnostic al markerilor amintiti rezulta din urmatoarele constatari54:
concentratiile serice crecute ale AFP si HCG persista cat timp exista tesut tumoral testicular activ in organism;
persistenta valorilor crecute dupa orhidectomie indica in mod categoric stadiul II sau III de boala;
persistenta valorilor crescute dupa limfadenectomie indica fie rezectie in-completa, fie stadiul III;
absenta interesarii ganglionare retroperitoneale in urma limfadenectomiei in-sotita de valori crecute ale acestor markeri indica stadiul III de boala (metas-taze osoase, cerebrale).
HCG urinar. Radioimunodozarea HCG in urina concentrata (urina din 24 ore) pare mai fidela decat dozarea serica (Javadpour N. 38), ceea ce permite o crestere a sensibilitatii metodei de dozare a bHCG. Studii clinice au aratat ca, la un numar semni-ficativ de pacienti cu HCG serica initial crescuta, la care, in urma citoreductiei chimice sau chirurgicale, s-au obtinut valori serice normale, determinarile RIA ale HCG urinar au continuat sa arate valori crescute tradand persistenta de tesut tumoral, fapt confirmat chirurgical si histologic13.
Lactic de hidrogenaza (LDH) este un test nespecific, avand o utilizare redusa42. Consta din mai multe izoenzime; izoenzima specifica TTG este izoenzima I care este produsa de toate tipurile de TTG. Specificitatea foarte redusa obliga la corelarea valorilor LDH cu a celorlalti markeri tumorali si cu contextul clinic.
Cresterile LDH sunt direct proportionale cu volumul tumoral, testul fiind mai informativ in stadiile avansate de boala cu volum tumoral mare (high volume disease). Astfel, s-au gasit valori crescute ale LDH in 8% din TTG stadiul I, 32% in stadiul II si 81% in stadiul III. Au fost utilizate in monitorizarea evolutiva a TTG, existand o relatie directa intre evolutia tumorii si a valorilor LDH.
Fosfataza alcalina placentara (PLAP) inregistreaza o mare rata de rezultate fals pozitive (35%) si fals negative, fiind mai putin utlizata54. A fost descrisa initial in cancerul bronhopulmonar, in timus si la fumatori. Inregistreaza valori crescute in seminom (40-l00%), cresterea fiind paralela cu stadiul extensiei la distanta: 30-50% in stadiul I, 100% in stadiile avansate.
b1 glicoproteina specifica sarcinii (SP 1) ar inregistra cresteri semnificative in carcinoame embrionare, teratocarcinoame si coriocarcinoame, niciodata in seminom42. Este secretata de sincitiotrofoblast, inregistrand valori crescute in sarcina, la gravida cu choriocarcinom gestational, precum si la 50% din cancerele testiculare metastatice (cu exceptia seminomului). Datorita faptului ca informatia oferita dubleaza valoarea HCG, determinarea acestei proteine nu este utilizata in practica.
Antigenul B5 poate creste in prezenta neoplaziilor (inclusiv in TTG)42, fiind prezent in cantitati reduse pe suprafata eritrocitelor la individul sanatos. Prezent la majoritatea TTG, ar avea valoare in monitorizarea evolutiei bolii sub tratament.
Neuron-specific enolaza (NSE)53 a fost izolata in formele de seminom-disger-minom si in teratoamele cu elemente neurale. Consecutiv are valoare diagnostica re-dusa, compensata insa de cea de monitorizare evolutiva a seminoamelor sub tratament.
Identificarea unor anomalii genetice/cromozomiale in TTG66, in special a izocro-mozomului 12i (12p) a deschis posibilitatea utilizarii acestora ca markeri tumorali citogenetici cu valoare atat diagnostica, cat si prognostica. Alte anomalii moleculare asociate TTG includ expresia oncogenei c-kit (in CIS si TGS) si hst-l (in TGNS)42, rafinand suplimentar diagnosticul. Acest lucru este valabil in special in cazul tumorilor disembrionare ale liniei mediane cu continut scrotal normal (TG primitiv extragonadale).
O listare a acestor anomalii cromozomiale neintamplatoare este relevata in tabelul 3. dupa Murty si Chaganti (1988) citati de Miron L.42
Tabel 3.
Tipul si
incidenta anomaliilor cromozomiale neintamplatoare in tumorile germinale
(dupa Murty V.V. si Chaganti R.S.K., Oncogene,
1994, citati de Miron L. 42)
|
Cromozomul |
Tipul mutatiei |
Incidenta |
|
1 |
deletia 1p 21-p36 |
16% |
|
4 |
pierdere / monosomie |
47% |
|
5 |
pierdere / monosomie |
52% |
|
6 |
deletie 6q 14-q 25 |
12% |
|
7 |
deletie / der 7q 11-q 36 |
20% |
|
8 |
castig / trisomie |
32% |
|
9 |
pierdere / monsomie |
39% |
|
11 |
pierdere / monsomie |
52% |
|
12 |
deletie 12 q 12-24 |
20% |
|
13 |
pierdere / monsomie |
55% |
|
18 |
pierdere / monsomie |
56% |
|
21 |
castig / trisomie |
35% |
In aceeasi referinta bibliografica42 se mentioneaza urmatoarele informatii privind mecanismele genetice implicate in transformarea maligna.
Studii citogenetice au probat existenta fenomenului de amplificare genica a unora sau mai multor gene si pierderea functiei mai multor gene supresoare tumorale. Retine atentia prezenta deletiilor cromozomiale ce implica mecanismul de pierdere a unor oncogene supresoare care in mod normal inactiveaza genele structurale (dominante) ce controleaza cresterea celulara.
Deletiile cromozomiale au dus la descoperirea unor gene supresoare in mai multe cancere. Este deja bine cunoscut rolul oncogenelor supresoare p53 si RB, ca si al DCC si NME ce par implicate si in oncogeneza TTG. Mutatiile genei TP 53 observate in peste 50% din cancerele umane pot determina pierderea controlului asupra ciclului celular si apoptozei, rezultatul final fiind proliferarea maligna. Date recente au implicat apoptoza ca mecanism al mortii celulelor maligne expuse actiunii chimioterapiei; s-a precizat o semnificativa crestere a proteinei p53 si inducerea apoptozei in populatia celulara de TG expusa la Etoposid. Mai mult, s-a sugerat ca aparitia unor mutatii in expresia p53 ar putea fi asociata cu instalarea fenomenului de rezistenta la Cisplatin, cu impact terapeutic major (Kurie J.M. et al.41). S-a sugerat astfel ca apoptoza indusa de TP 53 este importanta pentru efectul chimioterapiei cu Cisplatinum si ca mutatiile sale sunt una din cauzele chimiorezistentei la aceastaterapie in TTG.
Similar, pierderea functiei supresoare a oncogenei retinoblastomului RB1 prin deletie sau mutatie este implicata in patogeneza TTG42.
Deocamdata de interes experimental, restrans la cateva laboratoare de cercetare, studiile genetice in curs vor duce la descifrarea mecanismelor intime subcelulare ale patogenezei TTG, oferind implicit importante elemente diagnostice practice54.
Rezumativ, putem conchide ca (Proca E. 53) :
►cresterea izolata sau asociata a HCG si AFP, concomitenta unei mase tumorale scrotale si/sau retroperitoneale, mediastinale este patognomonica pentru diagnosticul de cancer germinal.
► orice TT asociind cresterea AFP contine un contingent de celule nonsemino-matoase si va trebui tratata ca atare.
► valoarea markerilor tumorali creste corespunzator volumului tumoral / stadiului de boala.
► concentratiile normale ale HCG si AFP nu exclud diagnosticul de TTG si nici cancerul rezidual.
► detectarea radioimunologica a gonadotrofinelor urinare este mai sensibila decat monitorizarea lor serica.
► identificarea imunohistochimica a HCG si AFP atesta originea germinala a tumorii, chiar daca diferentierea histologica nu permite acest diagnostic.
► AFP si HCG sunt crescute in 60% din stadiile I, in 70% din stadiile II si 90% din stadiile III ale TTG.
► titrul seric crescut al AFP si HCG dupa orhidectomie semnifica cancer rezi-dual, chiar in absenta evidentelor radiologice de diseminare.
► concentratiile foarte mari ale AFP ( > 500-l000 ng/ml) si bHCG ( > 1000 mUI/ml) semnific prognostic foarte rezervat de la inceput.
► cresterea valorii markerilor tumorali dupa o normalizare initiala, consecutiv terapiei, semnifica recidiva.
Aceasta ultima asertiune presupune interpretarea corecta a curbei evolutiei markerilor in raport cu timpul lor aparent de injumatatire. Aceasta notiune a fost introdusa in 1979 de Kohn, ca o corectie a timpului de injumatatire al unei TTG supuse terapiei adjuvante (radio / chimioterapie)42. Tumora ramane activa inca o perioada de timp de la debutul terapiei, descresterea markerilor in acest caz fiind o rezultanta a productiei (inca prezente) de markeri, eliminarii prin metabolizare si excretie, precum si distructiei tumorale, ceea ce face ca timpul real de injumatatire sa nu coincida cu cel biologic(in special pentru bHCG).
► determinarile repetate (saptamanale) ale markerilor au un rol extrem de im-portant in monitorizarea evolutiva a TTG sub tratament, descresterea lor fiind un indicator fidel al eficacitatii terapeutice.
Valoarea markerilor la momentul diagnostic are o indiscutabila valoare prog-nostica. Analize statistice multicentrice efectuate in scopul identificarii factorilor prog-nostici in formele metastatice de TGNS au permis distingerea unor subgrupe de pacienti cu prognostic favorabil (good risc) si nefavorabil (poor risc) pentru supravietuire. In termenii acestor date, valorile bHCG au o valoare importanta pentru aprecierea ras-punsului la tratament, a probabilitatii de recidiva si finalmente pentru supravietuire. Alte studii au creditat LDH cu aceeasi valoare prognostica42.
Valoarea prognostica acordata markerilor tumorali in TGNS este evidentiata in Consensul International de Clasificare a Factorilor Prognostici 50 la pacientii cu TTG elaborat de The International Germ Cell Cancer Colaborative Group (Mead si Stanning, 199542). Atfel, se considera:
► prognostic favorabil
bHCG < 1000 ng/ml ( < 5000 UI/l)
AFP < 1000 ng/ml
LDH < 1,5 x N (N= valori normale).
► prognostic nefavorabil
bHCG > 10.000 ng/ml ( > 50.000 UI/l)
AFP > 10.000 ng/ml
LDH > 10 x N .
► prognostic intermediar pacientii cu valori intre aceste doua categorii.
Principala utilitate a markerilor tumorali, ca instrument de stadiere, o constituie distinctia dintre boala localizata in scrot si cea diseminata. Din acest punct de vedere, o problema serioasa in decizia tereapeutica o constituie tumorile marker negative. In intentia de a creste sensibilitatea diagnostica, mai multi chirurgi au studiat nivelul markerilor in sangele venos recoltat din vena spermatica cu ocazia orhidectomiei. S-a constatat ca nivelul markerilor tumorali este mai crescut aici ca in sangele periferic, iar la unii pacienti prezenta acestora este detectabila doar aici42, 56!
Titrul seric crescut al markerilor tumorali, in absenta evidentei chirurgicale a diseminarii retroperitoneale si a evidentelor radiologice a determinarilor secundare, trebuie sa ridice suspiciunea dezvoltarii tumorii in sedii sanctuar: sistem nervos cen-tral sau testicul controlateral.
Recent, ca o confirmare a rolului major al markerilor tumorali in protocolul integrat de diagnostic, tratament si urmarire al TTG, American Joint Committee on Cancer (AJCC) si Union Internationale Contre le Cancer (UICC) au revizuit clasifi-carea TNM, stabilind, pentru prima oara, un sistem universal de stadiere. Este pentru prima data cand un sistem de stadializare TNM include valorile markerilor tumorali, ca urmare a inaltei lor relevante diagnostice si prognostice.
Diagnostic histologic
Explorarea chirurgicala a TT furnizeaza fara indoiala proba diagnostica (pozitiva si stadiala) peremptorie: criteriul histologic. Evident, sensibilitatea si specificitatea metodei sunt maxime. Se face prin examenul anatomopatologic al materialului (tumora, adenopatia, metastaza) recoltat operator prin:
ablatia tumorii primare
limfadenectomie retroperitoneala (LARP)
o de stadiere - in TTGNS stadiul I
o totala primara (neprecedata de chimioterapie) in TTGNS stadiile II A si II B
o totala secundara (precedata de chimioterapie) in TTGNS stadiul II cu mase reziduale post chimioterapie
exereze operatorii pentru determinari tumorale secundare pulmonare, mediasti-nale, cerebrale, vertebrale, etc.
biopsii operatorii ganglionare periferice, hepatice, etc.
Suspiciunea clinica de TT dicteaza obligatoriu orhidectomia radicala. Aceasta reprezinta ultimul pas in demersul diagnostic: examenul histopatologic, singurul criteriu de certitudine diagnostica. Acesta va trebui sa precizeze obligatoriu subtipul celular al tumorii germinale, extensia locala si prezenta / absenta invaziei limfo-vasculare, toate elemente histologice cu valoare prognostica, importante in incadrarea pacientului in varianta optima din protocolul integrat de tratament multimodal si urmarire.
Examenul anatomopatologic al piesei de orhidectomie radicala este obligatoriu, reprezentand singurul criteriu de certitudine diagnostica. Raportul anatomopatologic51 va preciza natura histologica si stadiul extensiei locale, prezenta invaziei limfo-vascu-lare, oferind informatii cu impact prognostic si terapeutic.
Orhidectomia inghinala cu clamparea primara, la orificiul profund al canalului inghinal a funiculului spermatic este gest diagnostic si terapeutic (Proca E.54). Sunt contra-indicate punctia biopsie percutanata sau ablatia pe cale scrotala avand in vedere riscul reci-divelor locale si modificarea rutei limfatice de diseminare cu agravarea prognosticului.
Piesa operatorie de orhidectomie radicala trebuie sa includa funiculul spermatic rezecat la orificiul profund al canalului inghinal (cu recupa la acest nivel) si anexele testiculului; ea trebuie sa fie examinata proaspata, masurata, cantarita si descrisa macro-scopic in toate detaliile. Se recolteaza pentru fixare fragmente din toate zonele tumorii, zone diferit colorate sau de consistenta inegala, din epididim si funiculul spermatic, inclusiv din recupa de bont funicular (Proca E.54).
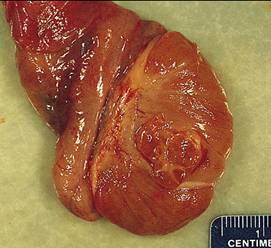
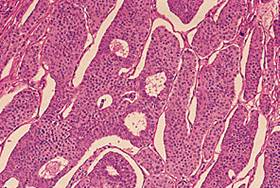
. 10. Examen anatomopatologic aspect macro/microscopic (cazuistica proprie)
Tumorile testiculare germinale provin histologic din celulele germinale primordiale, fiind impartite in doua categorii majore: seminomatoase (TTGS) care nu prezinta diferentiere histologica si non-seminomatoase (TTGNS) care prezinta diferentiere embrionara (carcinomul embrio-nar), extraembrionara (choriocarcinom, tumora sacului vitelin) si somatica (teratomul).
Tulburari ale migrarii celulelor germinale intre saptamanile 6-8 ale embriogenezei, de la sacul vitelin la gonade, explica localizarea de-a lungul liniei mediane a tumorilor ger-minale primitiv extragonadale in sedii precum: glanda pineala, gat, mediastin, retroperitoneu, regiunea sacrococcigiana. Daca transformarea maligna afecteaza celulele germinale migratoare, atunci TG sunt produse fie in sediile gonadice, fie in localizarile extragonadice.
Datele din literatura arata ca 40% din TTG ale adultului sunt seminoame pure, 15% tumori mixte asociind seminom si 45% sunt tumori non seminomatoase fara o componenta de seminom, ponderea formelor pure fiind foarte mica. cu exceptia carcino-mului embrionar. Ponderea mare a asocierilor germinale atesta deosebita capacitatea de diferentiere a celulelor stem. Acest lucru este demonstrat si de constatarea extrem de in-teresanta ca TTG pot metastaza cu alta structura histologica decat cea primara (in forma pura sau asociata)! precum si de posibilitatea metastazelor germinale de a se transforma spontan sau postcitostatic intr-o alta neoplazie (cel mai frecvent in sarcom).
TABEL 4.
Versatilitatea histologica a diseminarilor TTG in relatie cu histotipul TG primare -
201 cazuri consecutive (experienta Clinicii Fundeni9)
CE carcinom embrionar; S seminom; TC teratocarcinom; CC choriocarcinom
|
T |
N |
M |
Total |
|
S |
CE + S |
|
3 |
|
S |
TC + S |
|
2 |
|
CE |
TC |
|
4 |
|
CE |
CE + S |
|
2 |
|
CE + S |
TC |
|
1 |
|
TC |
|
CE + CC |
1 |
|
CE |
TC + CC |
|
1 |
|
|
|
|
14 cazuri |
Clasificarile histologice ale TT larg recunoscute sunt cea a lui Collins si Pugh Testicular Tumour Panell (1964), cu circulatie in Marea Britanie si Australia si clasificarea de circulatie mai larga a lui Friedman si Moore, modificata de Mostofi si Price (1976) si adoptata de O.M.S46. Le prezentam in continuare:
Clasificare Collins si Pugh (Testicular Tumour Panell) 8
1. Seminom
2. Teratom:
o teratom malign nediferentiat
o teratom malign trofoblastic
3. Tumori yolk sac (tumori de sinus endodermal)
4. Tumori combinate (combinatii de seminom cu teratom)
5. Tumori cu celule Sertoli
6. Tumori cu celule interstitiale
7. Orhioblastomul
8. Limfomul malign
9. Tumori diferite
10. Tumori metastatice
11. Tumori cu diagnostic incert
Clasificarea histologica OMS a tumorilor testiculare 51
1. Tumori germinale
A. Tumori germinale pure
- seminom
carcinom embrionar si tumora sinusului endodermic
- teratom
- choriocarcinom
B. Tumori germinale mixte
- carcinom embrionar cu teratom (teratocarcinom)
- carcinom embrionar cu seminom
- carcinom embrionar cu teratom si seminom
- teratom cu seminom
- orice combinatie cu choriocarcinom
2. Tumori ale cordoanelor sexuale si ale stromei gonadice
A. Forme bine diferentiate
- tumori cu celule Leydig
tumori cu celule Sertoli
tumori ale granuloasei
B. Forme intricate
C. Forme incomplet diferentiate
3. Tumori si pseudotumori continand atat celule germinale cat si ale cordoa-nelor sexuale si ale stromei gonadice
A. Gonadoblastoame
B. Alte tumori
4. Tumori variate
5. Tumori ale tesutului limfoid si hematopoetic
6. Tumori secundare
7. Tumori ale canalelor excretoare, tumori dezvoltate din retae testis, tumori epididimare, ale cordonului spermatic, ale capsulei, ale tesutului de susti-nere si anexelor
A. Tumori adenomatoide
B. Mezotelioame
C. Adenoame
D. Carcinoame
E. Tumori melanotice neuroectodermice
F. Tumori Brenner
G. Tumori ale tesuturilor moi
- rabdomiosarcoame embrionare
- alte tumori
8. Tumori neclasate
9. Leziuni pseudotumorale
A. Chiste epidermoide
B. Orhite nespecifice
C. Orhite granulomatoase nespecifice
D. Malakoplazie
E. Periorhita fibromatoasa
F. Granulomul spermatic
G. Lipogranulomul
H. Resturi suprarenaliene
I. Alte leziuni
Corespondenta nosologica intre subcategoriile histologice ale celor doua clasifi-cari principale ale TG este redata in urmatorul tabel de catre Horwich A., citat de Miron L. 42
Tabelul 5.
Histologia
TTG. Corespondenta nosologica intre cele doua clasificari principale
dupa Horwich A. Testicular germ cell tumor: An
introductory overview, in Testicular
Cancer: Investigation and Management, Second Ed., Chapman & Hall,
|
British Testicular Tumor Panel (Collins&Pugh) |
World Health Organization (Mostofi) |
|
Seminoame |
Seminoame |
|
Teratom diferentiat |
Teratom matur |
|
Teratom imatur |
|
|
Teratom malign cu diferentiere intermediara |
Teratom cu transformare maligna |
|
Carcinom embrionar si teratom |
|
|
Teratom malign nediferentiat |
Carcinom embrionar |
|
Teratom malign trofoblastic |
Choriocarcinom +/ carcinom embrionar si / sau teratom |
|
Tumori yolk sac |
Tumori yolk sac |
In ciuda caracterului exhaustiv al aceastor clasificari, vom retine ca - sub raportul practicii clinice - 95-97% din tumorile testiculare sunt maligne si germinale 54. Consecutiv, o tumora testiculara solida va fi considerata cancer pana la proba contrarie, fiind supusa orhidectomiei radicale (inghinale); examenul anatomopatologic urmeaza a stabili cu exactitate natura histologica a acesteia52!
Tipul celular de tumora germinala influenteaza decisiv riscul evolutiv si raspunsul terapeutic, finalmente prognosticul bolnavului.
In general, seminomul, chiar diseminat, raspunde foarte bine la radioterapie sau / si chimioterapie, inregistrand rate mari de supravietuire / curabilitate24,28,38 chiar in stadiul metastatic. In opozitie, choriocarcinomul inregistreaza evolutii galopante, rapid metastazante, total refractare terapeutic38, 54. Teratomul evolueaza foarte lent, local, timp indelungat, avand un potential metastazant mai redus38, 52. Carcinomul embrionar si tumora sacului vitelin poseda o capacitate de invazie mare si de metastazare rapida, necesitand scheme polichimioterapice extrem de agresive, cu rate mai mici de supravietuire in stadiile diseminante (Motzer R.J. et al., 1992 44).
Rezulta deci ca, diagnosticul histologic de seminom sau teratom pur, are un prognostic bun si necesita un efort terapeutic ativ mai redus. In opozitie, carcinomul embrionar pur sau asociat are un prognostic rezervat, iar choriocarcinomul un prognostic total infaust, ambele necesitand un efort terapeutic costisitor si foarte agresiv (Proca E., 1988 53, Javadpour N. 38).
Seminomul este cea mai frecventa TTG. In forma sa pura reprezinta 40% din TTG si inregistreaza o incidenta maxima intre 35-55 de ani34, 54. Este deasemenea prezent si in asociatiile germinale cu o incidenta de 15%. TTGS sunt foarte sensibile la radioterapie si chimioterapia specifica actuala15, 57.
Macroscopic este o tumora mare, ce creste testiculul in toate diametrele, pastrand forma ovoidului glandular. Pe sectiune prezinta aspect uniform, alb cenusiu, cu rare zone hemoragice si de necroza; prezenta acestora ridicand suspiciunea de elemente non-seminomatoase.
Microscopic este format din celule mari, rotunde, hexagonale, asemanatoare celulelor germinale primitive, cu citoplasma palida sau clara, cu nuclei centrali cu nucleoli evidenti; printre ele se gasesc infiltratie limfocitara si rare elemente gigante sincitiotrofoblastice mimand choriocarcinomul (10-20% din cazuri). Aceste celule nu contin gonadotrofina corionica umana si nu au semnificatie prognostica (Javadpour N.,1979 34). Varietati histologice: seminom spermatogonic (forma descrisa clasic), anaplazic si spermatocitic.
Seminomul anaplazic (10% din totalul seminoamelor) este caracterizat de pleio-morfism celular si nuclear, abundenta mitozelor si saracia stromei limfocitare. A fost descris de Mostofi ca o forma agresiva de seminom, putand fi confundat cu TGNS, diagnosticul diferential fiind facut de testele imunochimice. Contestat astazi ca entitate distincta, nu pare a avea o semnificatie prognostica particulara.
Seminomul spermatocitic (5% din totalul seminoamelor) are un prognostic mai bun, se intalneste exclusiv la varste inaintate (peste 65 de ani), nu este asociat altor tipuri celulare germinale (este doar pur), nu apare in sedii extragonadale sau in gonada ectopica si are o tendinta accentuata la bilateralitate42. Nu metastazeaza si are o relatie neclara cu alte TG, deoarece nu asociaza CIS, nu exprima PLAP ca celelalte seminoame, nu prezinta anomalii genetice comune TG54. Tumora este de dimensiuni mari, bine delimitata pe sectiune, de culoare gri sau galbena, cu suprafata de sectiune gelatinos mucoida, focarele de necroza hemoragica sunt extrem de rare, ades putand fi gasite mici chisturi cu lichid clar sau mucoid. Microscopic predomina pleiomorfismul, iar stroma limfocitara lipseste.
a) 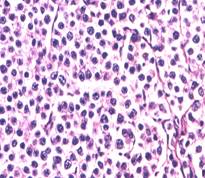 b)
b) 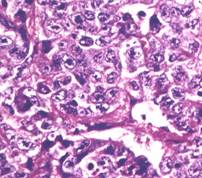
. 11. Tumori germinale aspect microscopic (preluat dupa Mostofi F. K. et al.46) :
a) seminom spermatogonic, b) carcinom embrionar
Carcinomul embrionar reprezinta aproximativ 40% din TT (25% in forma pura), este cea mai frecventa TG dupa seminom si inregistreaza incidenta maxima la pacientii mai tineri (20-35 ani), fiind exceptionala la copii sau la varstnici34. Potentialul agresiv al tumorii este foarte mare, evolutia sa fiind rapid invaziva si metastazanta. In clasificatia britanica corespunde teratomului malign nediferentiat8 .
Macroscopic este o tumora relativ mica, cu suprafata neregulata prin consistenta inegala, dezvoltata in plin parenchim testicular. Invazia in structurile adiacente este frecventa. Pe sectiune are aspect neomogen, alb cenusiu, cu zone intinse de necroza hemoragica.
Pattern-ul microscopic include o mare varitate de celule epiteliale dispuse glandular papilar, cu caracter anaplastic, cu structura embrionara heterogena. Este foarte agresiv, prezenta sa in histologia tumorii primare fiind considerata un factor de risc agravant pentru recidiva TTG stadiul I, alaturi de invazia vasculo-limfatica14, 44 si extensia la anexele testiculului.
Tumora sacului vitelin (yolk sac tumor, tumora sinusului endodermal sau carcinom embrionar infantil) este cea mai frecventa tumora testiculara la copil (60%)54, fiind extrem de rara la adult in forma pura. Pe sectiune tumora este neincapsulata, avand un aspect alb cenusiu, lobulat, cu consistenta inegala, moale, mucoida, alternand arii solide cu arii chistice.
Microscopic se descriu structuri tubulare sau glandulare anastomozate, adeseori cu aspect anastomozat microchistic sau papilar; uneori zone solide alterneaza cu zone papilare formand corpii Schiller Duval absolut caracteristici.
a) 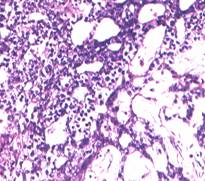 b)
b) 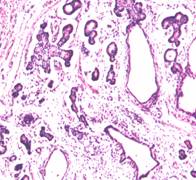
c) 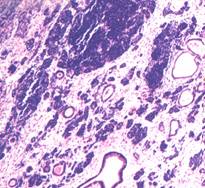 d)
d) 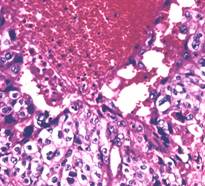
. 12. Tumori germinale aspecte microscopice (preluat dupa Mostofi F. K. et al.46) :
a) tumora de sac vitelin, b) teratom matur, c) teratom imatur, d) choriocarcinom cu carcinom embrionar
Teratomul are o incidenta mica in forma pura (5%), fiind mai frecvent asociat carcinomului embrionar (teratocarcinom)34. Este in general o tumora benigna. Dezvoltat la baieti in perioada prepubertara, se comporta ca tumora benigna, chiar daca in structura sa se gasesec si elemente mai putin mature, in timp ce la adolescenti si adulti are potential malign, metastazant chiar si atunci cand pattern-ul histologic54 denota aspect partial sau complet matur! Contine un potpuriu de structuri tisulare derivand din cele trei foite germinale. Macroscopic tumora este mare sau foarte mare, prezinta pe sectiune un aspect neomogen, pestrit, cu arii chistice, solide, cartilaginoase, osoase, sebacee, mucoase etc. Microscopic prezinta multiple structuri celulare specifice originii: glande mucoase (endoderm), tesut cartilaginos, muschi (mezoderm), chiste epiteliale scuamoase (ectoderm) cu diferite grade de diferentiere: matur, imatur, cancerizat. Este mai putin agresiv, cu potential metastazant mai redus. Forma pura nu raspunde la chimioterapie. Ades face parte dintr-o asociatie germinala, imprimand acesteia o evolutie mai putin agresiva. Din punct de vedere oncologic, teratomul prezinta un interes deosebit; desi histologic benign, poseda potential invaziv si metastazant, dupa cum metastazele TGNS pot sa se diferentieze spontan sau sub influenta chimioterapiei in teratom benign, iar TGNS primare nediferentiate pot metastaza ca teratom adult34, 54!
Histologic, sunt trei variante, in functie de gradul diferentierii54: teratom matur (compus din elemente tisulare adulte), imatur (compus din elemente cu diferentiere somatica similara cu acea a fatului, fara structura organoida) si cu transformare maligna. Ultimul contine in mod clar elemente de malignitate. Teratomul poate evolua spontan sau indus terapeutic (chimioterapie) spre alte malignitati13,22: sarcoame (frecvent rabdo-miosarcom), carcinoame, tumori neuroectodermice, leucemii si limfoame non-Hodgkiniene.
Choriocarcinomul afecteaza grupa de varsta foarte tanara, fiind foarte rar in forma pura (1%) si mai frecvent asociat (cand agraveaza prognosticul)34, 54. Este extrem de agresiv, practic incurabil. Metastazeaza, in principal, hematogen, dar si limfatic, adesea evitand spatiul retroperitoneal. Este insotit de cresterea foarte mare a b-HCG care sunt secretate de celulele sincitiotrofoblastice. Pacientii se prezinta cu boala metastatica avansata la primul diagnostic,decedand in scurt timp.
Sunt tumori mici (rar peste 5 mm Ø), moi, hemoragice (aspect inselator de hematom mai degraba decat de tumora!), rapid metastazante, care nu determina marirea de volum a testiculului54. Deoarece cresc foarte rapid, isi pot autosuprima circulatia sanguina cu regresia tumorii pana la necrobioza si formarea unei cicatrici testiculare reduse (relicva tumorii mama, a metastazelor concomitente sau burned-out tumor)52.
Microscopic este format din sincitiotrofoblasti si citotrofoblasti; prezenta ultimilor este obligatorie pentru diagnostic34, celule mari sincitiotrofoblastice putand fi regasite ca o componenta in structura tuturor TG, fara o semnificatie prognostica particulara. Celulele trofoblastice sunt dispuse sub forma papilara. Caracteristice choriocarcino-mului sunt masele hemoragice centrale, inconjurate de stratul celular periferic cu for-marea de pseudovili.
Tumorile germinale mixte reprezinta 35-55% din TTG si sunt compuse din doua sau mai multe subtipuri celulare germinale. Teoretic sunt posibile toate combinatiile, cu exceptia seminomului spermatocitic42. Unele combinatii apar mai frecvent; cea mai frecventa asociere este cea dintre teratom si carcinom embrionar, numita teratocar-cinom34,54. Analiza minutioasa a specimenului operator este extrem de importanta, precizarea exacta a prezentei si ponderii fiecarui tip celular germinal in asociatie avand valoare informativa pentru studiul metastazelor (este cunoscuta posibila histologie diferita) si pentru interpretarea unor posibile evolutii discordante sub tratamentul specific fata de natura anatomopatologica prezumata initial.
Carcinomul in situ (neoplazia germinala intratubulara) a testiculului repre-zinta o tumora germinala atipica, descrisa si asociata pentru prima oara cu dezvoltarea ulterioara a unui cancer invaziv de Skakkebaek in 197242. La ora actuala este considerat stadiul precursor al TGS si TGNS cu exceptia seminomului spermatocitic si al tumorii sacului vitelin42, 66. Asa cum aratam anterior, termenul de CIS este incorect, deoarece implica originea epiteliala a leziunii; termenul anglosaxon propus mai recent este cel de neoplazie germinala intratubulara (ITGCN). Se caracterizeaza prin proliferari intratubulare de celule mari, atipice, similare spermatogoniilor atipice, de care se deosebesc prin markerul antiPLAP. Leziunea a mai fost descrisa si in biopsiile testiculare facute pentru testicul criptorhid tratat sau nu (incidenta 8%), infertilitate (incidenta 1%) si testicul congener la pacienti cu TTG (incidenta 8%). Riscul de dezvoltare a unei TG invazive este estimat la 50% in primii 5 ani.
Vom incheia aceasta succinta trecere in revista a aspectelor histopatologice ale TTG reamintind existenta rara a cancerului germinal extragonadal (1-5%). Aparentul paradox al coexistentei unui cancer de tip germinal cu testicule normale se explica prin malignizarea unor celule restante de-a lungul traiectului de migrare al celulelor germinale embrionare de la sacul vitelin la gonade in perioada embrionara (Hainsworth J.D. et al., 1992 28). Cele mai frecvente localizari sunt retroperitoneale si mediastinale. Experienta clinica acumulata releva o incidenta de 1-5% din totalul TG, cu afectarea preponderenta a barbatilor intre 20-35 ani. Se asociaza frecvent cu sindromul Klinefelter, posibil datorita aceleiasi alterari cromozomiale.
Histologic se disting tumori seminomatoase si nonseminomatoase. Volumul tu-morii la momentul diagnostic este mare (Ø 20 cm), iar metastazele sunt prezente in 60-70% din cazuri (plaman, oase) ca rezultat al absentei barierei capsulei de organ. Prin-cipala contributie diagnostica o are tomografia computerizata si, in cazul TGNS, markerii tumorali, etiologia tumorii fiind precizata chirurgical, cu mentiunea ca in tumorile germinale primitiv extragonadice tentativa exerezei complete nu trebuie urmarita cu orice pret.
Alte tumori testiculare (in afara celor germinale) sunt foarte rare. Tumorile cordoanelor sexuale si ale stromei gonadale reprezinta aproximativ 4% din totalul tumorilor testiculare, iar cele mixte mai putin de 1%. Sunt exceptionale tumorile hematopoietice si determinarile secundare/metastazele testiculare. Le vom descrie (Ulbright M. T.,1976 68) succint in randurile ce urmeaza.
Tumora cu celule Leidig (2-3% din totalul tumorilor testiculare) survine in 20% din cazuri la copii cu varste cuprinse intre 5-l0 ani, insotindu-se de ginecomastie (totdeauna cu virilizare) sau pseudoprecocitate izosexuala (in 10% din cazuri). Este o tumora de dimensiuni mici, de regula nepalpabila. La adulti provoaca ginecomastie (bilaterala in 30% din cazuri) si se manifesta la varste cuprinse intre 30-60 de ani. Macroscopic, este o tumora circumscrisa, avand dimensiuni de 2-5 cm (in general sub 5 cm in diametru), cu aspect lobulat pe suprafata de sectiune, colorata cafeniu-galbui sau brun-cenusiu, rareori cu necroze sau hemoragii. Extensia extratesticulara este semnalata in 10-l5% din cazuri, iar bilateralitatea in 3% din cazuri. Microscopic, celule tumorale poligonale sau alungite, cu nuclei culosi si nucleoli centrali proeminenti, cresc in pattern difuz, alveolar, cordonal sau microchistic. Cristalele Reinke intracitoplasmatice se identifica numai in 40% din cazuri. La copii, tumora cu celule Leidig are o evolutie benigna. Aproximativ10% din cazurile dezvoltate la adult sunt maligne. Ca in majoritatea tumorilor cu celule endocrine, prezenta metastazelor tumorale (limfoganglioni, ficat, plamani, oase) reprezinta singurul criteriu cert de malignitate. Aspectele clinico-morfologice care prezic un potential biologic agresiv sunt: varsta inaintata; dimensiunile tumorale mari (peste 5 cm); marginile tumorale infiltrative; prezenta necrozelor tumorale; mai mult de 3 mitoze/10 HPF; invazia vasculara. Supravietuirea gnerala, in cazurile cu evolutie maligna, este de aproximativ 4 ani.
Tumora cu celule Sertoli (aproximativ 1% din totalul tumorilor testiculare) prezinta trei variante clinico-morfologice:
Tumora cu celule Sertoli, tipul comun apare la indivizi avand varste intre 15-80 de ani (in medie 45 de ani) ca masa tumorala testiculara circumscrisa, de dimensiuni in general mici (sub 4 cm), compacta, colorata albicios-galbui, fiind insotita ocazional de manifestari clinice induse de o impregnare estrogenica. Microscopic, prezinta celule tumorale cu nuclei ovalari formeaza structuri tubulare sau cordonale, sustinute de o stroma fibroasa, adesea hialinizata. Morfologic, evolutia biologica agresiva/maligna, intalnita in 10% din cazuri, poate fi suspicionata atunci cand tumora are dimensiuni mari (peste 5 cm) si exista necroze, atipii celulare severe, mitoze frecvente (mai mult de 5 mitoze/10HPF) si invazie vasculara;
Tumora cu celule Sertoli sclerozanta este o tumora benigna de dimensiuni mici (sub 1,5 cm), circumscrisa, colorata cafeniu-galbui, dezvoltata la indivizi cu varste cuprinse intre 18-80 de ani (varsta medie: 35 de ani), fara a fi insotita de manifestari endocrine;
Tumora cu celule Sertoli mari calcificanta este o tumora de dimensiuni mici (sub 2 cm), adesea bilaterala (in peste 25% din cazuri) si frecvent multifocala, colorata galben-cafeniu si consistenta nisipoasa datorita calcificarilor intratumorale. Se dezvolta la indivizi tineri (varsta medie: aproximativ 17 ani pentru formele cu evolutie benigna), uneori insotita de ginecomastie sau pseudoprecocitate izosexuala. 30% din cazuri apar la pacienti cu sindrom Carney sau sindrom Peutz-Jeghers. Foarte rare cazuri evolueaza malign (varsta medie a pacientilor: 39 de ani), potentialul biologic agresiv/metastazant corelandu-se cu: varsta (peste 25 de ani), dimensiunile tumorii (peste 4 cm), extensia extratesticulara, necroza tumorala, atipiile celulare, indexul mitotic (mai mult de 3 mitoze/10HPF) si invazia vasculara.
Tumora cu celule Sertoli-Leidig este extrem de rara, se insoteste de ginecomastie in 1/3 din cazuri, apare la varste diferite si, exceptional, prezinta o evolutie maligna.
Tumora cu celule de granuloasa este similara morfologic tumorii cu celule de granuloasa ovariana, dezvoltandu-se foarte rar la nivel testicular. Tipul juvenil se manifesta in general pana la varsta de 5 luni, se asociaza cu mozaicism X/XY, iar evolutia este benigna. Tipul adult se poate insoti de ginecomastie, se dezvolta la indivizi avand varste cuprinse intre 16-76 de ani, iar evolutia este benigna in general. Formele maligne (exceptionale) se caracterizeaza prin dimensiuni tumorale mari (peste 7 cm), necroze hemoragice intratumorale si invazie vasculara.
Fibromul testicular este exceptional si se dezvolta din celulele stromei gonadale. Pacientii, in varsta de 28-35 de ani, prezinta un nodul tumoral testicular ferm, compact, albicios, uneori avand dimensiuni mai mari de 4 cm. Evolutia este totdeauna benigna.
Tumori ale cordoanelor sexuale si ale stromei gonadale mixte si neclasificate: Sunt tumori rare, de dimensiuni variabile, care se dezvolta la indivizi de varste diferite, manifestandu-se la copii in 50% din cazuri. Se insotesc de ginecomastie in 15% din cazuri. Numai 20% din tumorile dezvoltate la adulti prezinta o evolutie maligna (tumori dezvoltate la varstnici, cu dimensiuni mari, pattern invaziv de crestere, necroze tumorale, atipii nucleare, mitoze frecvente si invazie vasculara).
Tumori mixte ale celulelor germinale, cordoanelor sexuale si stromei gonadale
Gonadoblastomul (tumora Morris-Scully) este o tumora mixta, alcatuita din celule germinale, similare celor seminomatoase, si celule ale cordoanelor sexuale, probabil celule Sertoli. Sunt tumori colorate cafeniu-galbui, nisipoase pe suprafata de sectiune si bilaterale in 1/3 din cazuri. Se dezvolta totdeauna la pacienti cu gonade disgenetice si sindroame intersexuale (20% prezinta fenotip masculin si 80% fenotip feminin). Unii autori o considera o forma in situ de tumora cu celule germinale, deoarece in 50% din cazuri poate evolua catre transformare intr-o tumora cu celule germinale, in special de tip seminom, rareori (8% din cazuri) de tip carcinom embrionar sau tumora vitelina. Tratamentul consta in orhiectomie bilaterala, evolutia fiind benigna la pacientii care nu prezinta componenta cu celule germinale invazive.
Limfomul malign testicular reprezinta 5% din totalul tumorilor testiculare si 50% din tumorile testiculare ale barbatului varstnic (peste 60 de ani). Majoritatea sunt determinari secundare in cadrul unui limfom malign generalizat. In 20% din cazuri, afectarea testiculara este bilaterala, frecvent metacrona. Este o tumora macroscopic similara seminomului, in sensul ca este compacta, colorata roz-albicios, de consistenta encefaloida, singura deosebire constand in faptul ca, mai frecvent, este extinsa extratesticular. Microscopic, majoritatea limfoamelor maligne testiculare sunt limfoame maligne non-hodgkiniene cu celule mari de tip B, mai rar limfoame maligne anaplazice cu celule mari; la copil au fost semnalate cazuri de limfom Burkitt. Cel mai important factor de prognostic este stadiul tumoral.
Plasmocitomul testicular, de cele mai multe ori, reprezinta o manifestare a unui mielom multiplu la pacienti in jurul varstei de 55 de ani.
In leucemii, afectarea testiculara este frecvent bilaterala si apare in 40-65% din cazurile de leucemii acute si in 20-35% din cazurile de leucemii cronice. Sarcomul granulocitic (tumora mieloida extramedulara) este descris si la nivel testicular.
Chistul epidermoid testicular este exceptional. Se dezvolta la indivizi tineri (20-40 de ani) ca o masa chistica uniloculata care contine material albicios lamelar (keratina). Evolutia este totdeauna benigna. In parenchimul testicular invecinat nu se identifica niciodata aspecte de neoplazie intratubulara cu celule germinale. Trebuie distins de teratom si de chistul dermoid.
Carcinoidul este exceptional o tumora testiculara primitiva. De regula, reprezinta o componenta a unui teratom sau o metastaza a unei tumori neuroendocrine extratesticulare.
Tumorile mezenchimale testiculare sunt extrem de rare. Au fost descrise forme benigne (leiomiom, neurofibrom, hemangiom) si forme maligne (osteosarcom, fibrosarcom, leiomiosarcom, rabdomiosarcom, sarcom Kaposi).
Pot evolua cu determinari secundare/metastaze (in ordinea frecventei) carcinomul prostatic, carcinomul pulmonar, melanomul malign, carcinomul pancreatic, gastric si colonic, carcinomul hepatocelular, carcinomul renal si tumori neuroendocrine. 20% din cazuri sunt bilaterale, iar pattern-ul de crestere poate fi multinodular sau difuz.
TABEL 6.
Profilul histologic al tumorilor testiculare experienta Clinicii Fundeni9
(1976-l993)
1. Tumori benigne : 3 cazuri
- hemangiom 1 caz
- carcinoid 2 cazuri
2. Tumori maligne : 208 cazuri
A.Tumori non-germinale 7 cazuri
limfom 4 cazuri
leydigiom 2 cazuri
androblastom 1 caz
B.Tumori germinale 201 cazuri
a/ pure 135 cazuri
seminom 78 cazuri
carcinom embrionar 47 cazuri
teratom 6 cazuri
tumora de sac vitelin (yolk sac) 2 cazuri
choriocarcinom 2 cazuri
b/ mixte 66 cazuri
teratocarcinom 36 cazuri
teratocarcinom+seminom 17 cazuri
seminom+carcinom embrionar 11 cazuri
choriocarcinom+altceva 1 caz
yolk sac tumour+altceva 1 caz
Diagnostic diferential
Lista afectiunilor ce trebuiesc excluse (Proca E., 1999)54 cuprinde:
1. tumefactii scrotale dureroase: orhiepididimita acuta nespecifica, epididimita acuta nespecifica, epididimita cronica nodulara, orhita granulomatoasa, tor-siunea de funicul spermatic sau hidatida Morgagni (frecvente la copil), hernia inghinoscrotala incarcerata sau strangulata
2. tumefactii scrotale nedureroase: hidrocel, hematocel, spermatocel, chist epidi-dimar, varicocel, periorhita nodulara
3. tumori paratesticulare: tumori maligne sau benigne de epididim sau funicul spermatic.
Dupa caz, anamneza atenta, examenul clinic local minutios, ecografia scrotala (inghinala), in unele situatii proba terapeutica scurta (antibioterapie) si in ultima instanta explorarea chirurgicala pe cale inghinala cu orhidotomie exploratorie/orhidectomie radicala si raportul examenului histopatologic al piesei de exereza radicala ne vor feri de eroarea diagnostica 52.
In cele ce urmeaza vor fi prezentate numai tehnicile care utilizeaza antigenii (alergenii) in "starea lor obisnuita", adica testele cutanate si testel [...] |
Acest sindrom de hipen-eaetivitate bronsica, observat la persoane cu o predispozitie constitutionala particulara, pune adesea probleme di-ficiile de d [...] |
Dispneea reprezinta simptomul major, dar nu patogonomonic, al insuficientei respiratorii. Ea exprima, in primul rind, dar nu obligatoriu, o su fer [...] |
Copyright © 2010 - 2025
: eSanatos.com - Reproducerea, chiar si partiala, a materialelor de pe acest site este interzisa!
Informatiile medicale au scop informativ si educational. Ele nu pot inlocui consultul medicului si nici diagnosticul stabilit in urma investigatiilor si analizelor medicale la un medic specialist.
Termeni si conditii - Confidentialitatea datelor - Contact