|
|
Hepatita c este
o problema de sanatate ce a aparut dupa 1990, odata cu descoperirea acestui
virus. Anterior acestei date exista notiunea de hepatita
non-A, non-B. Reprezinta o problema importanta
deoarece descoperim acum cazuri de hepatita cronica datorate
unor transfuzii efectuate inainte de cunoasterea si testatrea acestui virus.
Infectia cu virusul hepatitic C ( VHC ) afecteaza actual ~ 170 de milioane locuitori in SUA si Europa, circa 75% din ei dezvoltand infectie cronica exprimata ca hepatita cronica, ciroza hepatica ( 20- 30% ) sau carcinom hepatocelular. Desi prevalenta infectiei in populatia generala nu este foarte bine cunoscuta se identifica zone de endemie:
Pentru ca
infectia cu VHC sa se extinda este necesar sa existe sursa de infectie,caile de transmitere si masa receptiva. Sursa de infectie
este reprezentata de subiectul viremic ( bolnav/
donator de sange ). Receptivitatea populatiei la infectie este generala
avand in vedere ca nu exista o vaccinare impotriva hepatitei C. Transmiterea
infectiei se face pe cale percutana, transfuzional sau non-transfuzional, sau
pe cale non-percutana, oculta.
Transmiterea percutana transfuzionala. VHC a fost
considerat la inceputul aniilor `90 responsabil de ~95% din hepatitele
posttransfuzionale ( HPT ). Screeningul corect al sangelui
a condus la o scadere dramatica a HPT, dar riscul se mentine in ariile de
inalta prevalenta, in zonele in care nu s-a renuntat la donatorii platiti si in
cele in care se lucreaza cu teste diagnostice neperformante. Riscul este crescut cand sunt necesare transfuzii masive si/sau
iterative. Derivatele de sange obtinute din pool-uri plasmatice, in special
concentratele factorilor de coagulare,prezinta un risc
inerent de infectie.
Transmiterea percutana non-transfuzionala este
responsabila de infectiile la toxicomani, hemodializati, personalul medical,
pacienti cu interventii chirurgicale in antecedente, netransfuzati ca si de
infectiile nozocomiale semnalate in serviciile oncologice/centrele de
plasmafereza.
Transmiterea non-percutana/ oculta pare a fi de tip sexual si perinatal. Calea
sexuala pare mai putin importanta decat se credea, dovada procentajul mic de
infectii la homosexuali anti-HIV - urmariti prospectiv. Infectia la partenerii
heterosexuali ai pacientilor este rara. Transmiterea
perinatala demonstrata se coreleaza cu titruri mari
ale viremiei, dar este rara la nou nascutii din mame anti-HIV.
Masa receptiva este foarte larga, identificandu-se in ea grupe populationale cu
risc si anume: personalul medical si paramedical din institutiile publice si
private, toxicomanii, recipientii de sange sau organe (
talasemici, hemofilici, operati pe cord deschis, transtati renal,
hemodializati, prostituatele, mai ales cei anti-HIV +.
Virusul
hepatitic C a fost descoperit de catre Q.L. Choo ( 1988 ) siM.Houghton ( 1989 )
de la laboratoarele Emeryville, California, in colaborare cu B. Bradley de la
CDC - Atlanta. Utilizand tehnici de clonare moleculara,
descopera VHC la cimpanzeii infectati cu serul provenit de la bolnavii cu hepatita
non-A, non-B. VHC este un virus ARN liniar,
monocatenar, cu polaritate pozitiva, alcatuit din 9500 de nucleotide a carui
genom este organizat similar cu cel al flavivirusurilor si pestivirusurilor. HCV constituie propriul gen in familia Flaviviridae. Genomul
HCV contine un singur cadru deschis de citire care
codeaza o poliproteina virala de ~3000 de aminoacizi. Capatul 5 al genomului
este alcatuit dintr-o regiune netradusa adiacenta genelor pentru proteinele
structurale, miezul nucleocapsidic proteic si doua glicoproteine de invelis, E1
si E2/NS1, regiunea netradusa de la capatul 5 si gena pentru miez sunt foarte
bine conservate in genotipuri,dar proteinele de invelis sunt codate in regiunea
hipervariabila, care variaza de la un izolat la altul.Aceasta permite virusului
sa evite mecanismele imunologice ale gazdelor indreptate impotriva proteinelor
accesibile din invelisul viral. Capatu 3 al al genomului contine genele pentru
proteinele nonstructurale.Au fost identificate, prin secventializare a
nucluotidelor, cel putin 6 genotipuri distincte ale HCV precum si subtipuri ale
genotipurilor. Datorita deosebirii izolatelor HCV in cadrul genotipului sau
subtipului si la aceeasi gazda, este imposibila
definirea unui genotip distinct, aceste diferente intragenotipice referindu-se
la termenul de semispecie. Diversitatea genotipica si a semispeciilor HCV,
rezultand din rata inalta de mutatie a acestuia,
interfereaza cu imunitatea efectiva umorala.
Au fost pusi in evidenta anticorpi neutralizati ai HCV, dar ei tind sa aiba o viata scurta si infectia cu HCV nu induce
imunitate durabila fata de reinfectia cu diferite izolate virale sau chiar fata
de acelasi izolat viral. Ca urmare, nici imunitatea
heterologa nici cea homologa nu se dezvolta dupa infectia acuta cu HCV.
Unele genotipuri HCV au o distributie universala, in timp ce
altele sunt limitate la anumite zone geografice. In plus, au
fost semnalate diferente patogenice si in raspunsul la terapia antivirala a
genotipurilor; oricum impactul biologic al diferentelor genotipurilor si
semispeciilor ramane incomplet elucidat.
 hepatita c" v:shapes="_x0000_i1025">
hepatita c" v:shapes="_x0000_i1025">
ura 5. Organizarea genomului VHC si proteinele asociate ( 8 ).
Patogenia HC
tip C, desi necunoscuta, este probabil, rezultanta
conflictului intre agresivitatea virala, exprimata ca efect citopatic, si
raspunsul imun al organismului la agresiune, probabil de tip citotoxicitate
directa.
Localizarea virala. Detectia ARN VHC
prin hibridizare in situ si PCR a demonstrat prezenta ARN in citoplasma
hepatocitara si rareori nuclear/perinuclear sau in alt tip de celula decat
hepatocitul. Celulele infectate cu dispozitie periportala/acinara sunt situate
langa ariile de piecemeal/spotty necrosis si sunt mai numeroase in infectia
tardiva ( hepatita periportala sau
ciroza ). Localizarea virala ( cu mari variatii de la un acin la altul )
demonstraza ca acinii ARN VHC + au majoritetea hepatocitelor infectate cu cel
putin 20 de copii virale/celula si aceiasi acini au activitate maxima
inflamatorie.
Reactiile inflamatorii. In HC tip C s-au
evidentiat histologic frecvent: foliculi limfoizi portali, leziuni de ducte
biliare, steatoza hepatica si prezenta corpilor Mallory. Foliculii limfoizi din
spatiile porte sunt de tip B, activi, cu o mixtura de
limfocite T periferic. Se identifica anterior aparitiei
cirozei, in aceasta din urma fiind inlocuiti de agregate limfoide demonstrand
fenotipul T si dispuse in septuri conjunctive. In privinta
necroinflamatiei, se constata ca limfocitele periportale din jurul foliculilor
B sunt reprezentate egal de CD 4+ si CD 8+, primele dominand in zonele de
piecemeal, ultimile in zonele de spotty necrosis, alaturi de limfocitele T de
memorie. Predominanta limfocitelor CD4+ sugereaza postura de pacient/martor la un proces inflamator autoimun. Celule Tc au fost gasite
asociate hepatocitelor apoptoice Fas + / core + in ariile de piecemeal
necrosis. Aceste limfocite recunosc epitopi core si de
invelis.
Raspunsul la terapie. Observatii
asupra tratamentului cu alfa/ beta- IFN in
hepatitele acute C au demonstrat reducerea progresiei la cronicitate.
Responsivii si-au redus nivelul de AT, inflamatie portala/acinara, numarul de
celule CD 8+ intraacinare si imunopozitivitatea histologica pentru antigenele
VHC, ca si nivelurile serice/hepatice ale ARN VHC. Nu s-a remarcat reducerea
fibrozei decat intr-un numar redus de cazuri si in grad limitat. De aici reiese
ca reducerea activitatii bolii este datorata lizei
celulelor infectate indusa de IFN mai degraba decat imunomodularea.
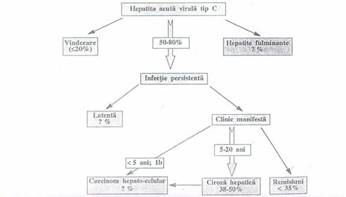
Istoria naturala a infectiei cu VHC. Infectia acuta VHC evolueaza in majoritatea cazurilor asimptomatic. Aspectul de hepatita acuta fulminanta este rar intalnit. Boala poate imbraca o forma acuta severa atunci cand infectia se grefeaza pe fondul unei hepatopatii cronice necunoscute, cand se produce o coinfectie VHB-VHC sau la primitorii de transt hepatic. Evolutia este marcata de procentul mare al cronicizarii bolii hepatice ( 70-80% ) si de dezvoltarea cirozei ( 20% ) dupa un interval mediu de 3 decenii. Carcinomul hepatocelular ( 3-4% ) si ciroza explica marea majoritate a deceselor la cei cu hepatita de aceasta etiologie.Factorii de prognostic negativ privind rapiditatea progresiei bolii sunt: genotipul I b, nivelul ridicat al viremiei si gradul diversitatii genetice a virusului, transmiterea transfuzionala a VHC, imunodeficienta, coinfectia cu VHB sau HIV si consumul abuziv de alcool.
 hepatita c" v:shapes="_x0000_i1026">
hepatita c" v:shapes="_x0000_i1026">
ura 6. Istoria naturala a infectiei cu VHC ( 9 ).
Tabloul clinic al hepatitei c este cel mai adesea sters sau absent. Un semn destul de caracteristic este astenia persistenta, nejustificata de efortul fizic sau psihic depus; alte manifestari clinice sunt reprezentate de fatigabilitate, inapetenta, mialgii, dureri in hipocondrul drept. Uneori poate sa apara un sindrom dispeptic nesistematizat. Alteori, in hepatita C pot aparea manifestari extrahepatice, considerate ca expresie a unor tulburari imunologice: purpura trombocitopenica, artralgii, poliarterita nodoasa, crioglobulinemia mixta, sindromul Sjogren, tiroidita autoimuna, glomerulonefrita membranoasa, hepatita autoimuna si diverse manifestari cutanate de tip lichen , sialadenita, ulceratii corneene.
Se suspecteaza o hepatita C la:
Confirmarea vine din coroborarea datelor oferite de istoricul medical, examenul fizic, TFH, biopsie hepatica si teste serologice virale.
Evolutia
bolii este de lunga durata, considerandu-se ca timpul
mediu de la infectie si pana la ciroza este de ~20 de ani, adeseori chiar mai
mult. Evolutia depinde de prezenta si nivelul viremiei,
genotipul viral, boli asociate, varsta, sexul. Remisiunea histologica
spontana este neobisnuita. Procentajul de dezvoltare a
cirozei pare sa creasca paralel cu durata urmaririi.
Carcinomul hepatocelular apare in procentaj mai mare dacat in cazul infectiei
cronice cu virus hepatitic B. Factorii influentand rata de progresie de la hepatita
la ciroza include: varsta la momentul infectiei, modul de contagiune, durata
infectiei, gradul leziunilor histologice la biopsia initiala, statusul imun al
pacientului si genotipul viral.
Progresia bolii este variabila si nu totdeauna
ordonata si secventiala.
Pacientii pot evolua de la hepatita portala/periportala direct
la cancer hepatocelular,fara a dezvolta ciroza
hepatica, mai ales la cei infectati cu genotipul 1b. Ciroza hepatica nu pare sa conduca la insuficienta hepatica subfulminanta la
toti pacientii.
Majoritatea pacientilor cu infectie cronica cu virus C au histologie hepatica
anormala, dar sunt aparent sanatosi, iar cei care au TFH normale, pot avea
leziuni histologice substantiale.Viremiile inalte si genotipul viral agresiv (
1b ) ar fi implicate in evolutia mai severa si prognosticul defavorabil al
pacientilor.
Infectia cu virus hepatitic C posttranst hepatic a fost recunoscuta dupa
1990 la aproximativ 25% din pacienti. Nivelul viremiei creste
de peste 15 ori posttranst. Evolutia transtatilor reinfectati cu
virusul hepatitic C este grevata de o supravietuire
redusa, sesizabila dincolo de 3 ani de la transt. Studiile histopatologice
au relevat leziuni histologice pe grefon la aproximativ 50% din pacienti in
primul an posttranst. Exista un subset de pacienti
transtati, reinfectati precoce, cu boala agresiva survenind la mai putin de
6 luni posttranst, care conduce la pierderea grefonului si exit (<5%).Nu
se stie inca exact daca severitatea leziunilor pe grefon este rezultatul
efectului citopatic viral sau raspunsului imun accelerat la pacienti
imunodeprimati.
Complicatiile posibile sunt: ciroza hepatica ( destul de frecvent ), hepato-carcinomul ( cel mai adesea pe fond de ciroza ), purpura, glomerulonefrita cu evolutie spre insuficienta renala cronica, precum si alte boli autoimune ( tiroidiene, cutanate).
Tratamentul hepatitei c cuprinde masuri generale si medicatie.
Masurile generale pentru un astfel de bolnav cuprind
un regim de viata apropiat de cel al unui individ normal. Activitatea fizica
usoara ( miscarea ) nu va fi contraindicata. Repausul la pat in mod prelungit nu a dovedit a aduce beneficii. In
formele usoare si moderate, bolnavul poate sa-si continue
activitatea profesionala, mai ales in mesrii fara eforturi fizice deosebite. Se
va contraindica in mod absolut consumul de alcool,
datorita efectului sinergic hepatotoxic.
Dieta este apropiata de cea a unui individ
normal, recomandandu-se aport suficient de proteine, vegetale si fructe.
Administrarea de medicamente va fi contraindicata pe
cat posibil, din cauza efectului hepatotoxic al multor medicamente. Medicamentele hepatotrope nu modifica evolutia bolii si
nu au efect antiviral.
Ele au mai mult un efect placebo, de aceea ele vor fi
folosite discontinuu si cu discernamant. Se pot folosi: Essentiale forte,
Endonal, Silimarina, Hepaton, Metospar,etc.
Medicatia antivirala reprezinta la ora actuala baza terapiei in hepatita
C ,
efectuandu-se cu interferon, derivati ai acestuia si analogi nucleozidici-
Ribavirina. Scopul tratamentului este cel al eradicarii VHC exprimat prin
raspuns sustinut ( 24 48 saptamani de la sistarea
tratamentului ): normalizarea aminotransferazelor si negativarea ARN VHC ( PCR
negativ ), cu imbunatatirea tabloului histologic.
Interferonii ( IFN ) reprezinta un grup de glicoproteine produse de celulele nucleate stimulate viral sau prin inductori ce apartin clasei citokinelor; ei manifesta proprietati antivirale, imunoreglatorii si antiproliferative. IFN sunt desemnati ca alfa, beta si gama.
IFN exercita actiuni biochimice si celulare directe si indirecte. Dupa legarea de receptorii membranari, actiunile directe
sunt rapid initiate prin semnale trans-citoplasmatice, posibil mediate de
produsii metabolismului acidului arahidonic. Actiunile indirecte pot fi mai
lente ca dezvoltare si dependente de interactiunea cu alte citokine si/sau
factori de crestere.Efectul antiviral se explica prin inductia oligoadenilat
sintetazei ( OAS ) sau proteinkinazei P1 ( PKP1 ).
Tratamentul cu alfa-IFN se recomanda pacientiilor cu HC virala tip C,
indiferent de varsta si existenta sau nu a unui episod HVA simptomatic, daca
este demonstrata activitatea biologica ( ALT anormale
), probata serologic infectia ( anti-VHC + in teste ELISA de generatia a 3-a)
sau/si viremia ( ARN VHC + ) si stabilita histologic existenta necroinflamatiei
cel putin moderata/severa si nivelul mediu al fibrozei ( scor Knodell >6).
Contraindicatiile tratamentului
antiviral cu interferon:
Principalele
efecte adverse ale alfa - IFN sunt:
minore/ modeste sindrom pseudogripal,astenie,mialgii,cefalee/migrene,
anorexie, greata, scadere ponderala, diaree, dureri abdominale, iritabilitate,
insomnii, alopecie, eritem cutanat, neutropenie, trombocitopenie; severe -
depresie, delir, agitatie, criza epileptica, distiroidie,
cardiopatie,manifestari autoimune.
Monitorizarea tratamentului. La initierea tratamentului cu alfa-IFN, pacientii vor
avea un bilant complet care va permite argumentarea
indicatiei terapeutice, evaluarea severitatii bolii hepatice, excluderea altor
maladii hepatice/extrahepatice asociate. In cursul perioadei
de tratament, pacientii vor fi monitorizati spre a vedea eficienta acestuia si
a semnala efectele adverse severe care impun ajustarea dozei, intreruperea
temporara/ definitiva a tratamentului. Ritmiul de supraveghere va fi lunar in cursul tratamentului, pentru ALT, AST,
hemograma. ARN VHC ( PCR ) calitativ, exprimat ca ( + ) sau ( - ), testat cu
Amplicor va fi reluat dupa 3 luni, preferabil printr-un test cantitativ de tip
bDNA-Quantiplex si la 6 luni de la finele tratamentului. TSH va
fi dozat la intervale de 3 luni. In perioada postterapeutica, bilanturile se
vor face la 2 luni in primul semestru, ulterior la 3 luni pana la finele unui
an de supraveghere, urmand apoi un bilant annual, timp de 3-5 ani. Factorii
predictivi pentru raspuns terapeutic bun sunt urmatorii: varsta tanara ( sub 40 de ani ); absenta cirozei si un scor histologic mic
al fibrozei; genotipul II sau III; incarcarea virala joasa ( sub 2 milioane
copii/ml. ); sexul feminin.
Terapia combinata cu derivati ai interferonului- Peg Interferon si
Ribavirina ( analog nucleozidic ) este standardul
actual al terapiei hepatitei c. Peg Interferonul este un interferon pegylat,
ceea ce permite degradarea si eliminarea lenta a acestuia si deci posibilitatea
mentinerii unui nivel plasmatic crescut chiar in conditiile administrarii lui
saptamanale. Pegylarea este procesul de atasare a uneia sau mai multor molecule
de polietilen glicoli ( PEG ) unei alte molecule cum
ar fi o proteina terapeutica.
Polietilen glicolii sunt polimeri inerti, hidrosolubili,
netoxici rezultati in urma legarii mai multor subunitati de etilen-oxid.
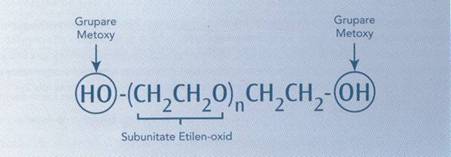 hepatita c" v:shapes="_x0000_i1027">
hepatita c" v:shapes="_x0000_i1027">
.7.Structura polietilen glicolilor ( 6).
Exista un mare numar de molecule de PEG care difera prin conuratie ( liniara sau ramificata ) si prin greutate moleculara. Moleculele de PEG cu diferite greutati moleculare au proprietati fizice foarte diferite. De exemplu, in forma purificata si neconjugata, moleculele mici de PEG ( PEG 200 ) sunt lichide uleioase, pe cand moleculele mari de PEG ( PEG 8000 ) au consistenta solida. In cazul enzimelor, activitatea enzimatica a fost impiedicata si timpul de injumatatire al proteinelor pegylate s-a prelungit. Moleculele de PEG prezinta proprietati importante care pot conferii efecte benefice proteinelor terapeutice.
Astfel,
atunci cand PEG este atasata unei proteine terapeutice
ii confera acesteia hidrosolubilitate, proprietati protective si non
imunologice.
IFN nepegylat se administreaza subcutanat; administrarea orala nu este posibila din cauza degradarii la nivel intestinal. Dupa
administrarea injectabila IFN este:
Asrfel, IFN
are o durata de actiune foarte scurta. Pentru a realiza
concentratii sanguine terapeutice eficiente de IFN pe toata durata
tratamentului, teoretic acesta ar trebui administrat de mai multe ori pe zi.
Dar, chiar si administrarea unica zilnica nu este convenabila,
este costisitoare si poate fi greu tolerata. In cazul
tratamentului hepatitei C se recomanda administrarea IFN de trei ori pe
saptamana. Aceasta schema terapeutica reprezinta mai mult un compromis decat un ideal si duce la fluctuatii mari ale concentratiilor
plasmatice de IFN de-a lungul saptamanii.
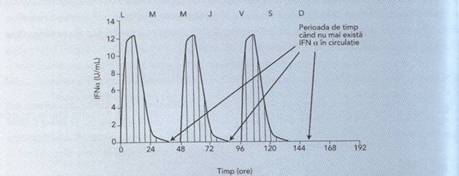
Concentratiile plasmatice maxime de IFN se realizeaza in ziua
administrarii. In zilele dintre administrari, concentratiile plasmatice
descresc dramatic, iar in weekend nu mai exista IFN in circulatie. In
perioadele cand nu mai exista IFN in circulatie, virusul hepatitic se poate
replica necontrolat, aceasta putand duce la rebound viral si apare riscul
rezistentei virale. In plus, fluctuatiile concentratiilor plasmatice de IFN
sunt corelate cu efecte adverse neplacute de tipul astenie, cefalee, febra sau
mialgii, efecte care pot determina pacientul sa intrerupa tratamentul cu IFN.
 hepatita c" v:shapes="_x0000_i1028">
hepatita c" v:shapes="_x0000_i1028">
.8.Concentratii serice ale IFN pe parcursul unei saptamani cu 3 administrari ( 6 ).
Pegylarea are potential de a imbunatatii farmacocinetica si farmacodinamica IFN si, de aceea, se pot evita fluctuatiile concentratiilor plasmatice si regimurile de dozaj incomode ale IFN conventional. Scopul fundamental al pegylarii oricarei proteine terapeutice este de a optimiza la maxim farmacocinetica acesteia, in acelasi timp pastrandu-i activitatea. In acest sens, gradul de optimizare este specific fiecarui produs si variaza in functie de:
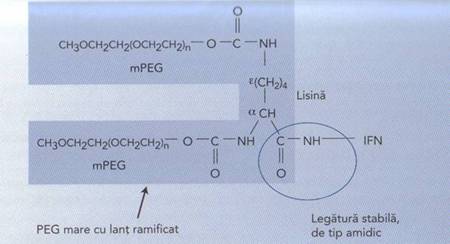
In fiecare portiune terminala a moleculei de PEG se afla o grupare hidroxil ( - OH ). Ambele grupari terminale sunt active chimic, permitand atasarea PEG la o proteina. Pentru a se evita legarea incrucisata si agregarea se prefera pastrarea unei singure grupari active la un singur capat. Acest lucru se obtine prin convertirea unei grupari hidroxil terminale intr-o grupare metoxi ( CH3O ) inactiva, formand monometoxi PEG ( mPEG ). Avantaje semnificative in tehnologia pegylarii s-au obtinut prin folosirea moleculelor ramificate de mPEG, in care lanturile de PEG sunt legate pentru a forma molecule cu greutate mare ( 60 KD ). S-a obtinut o molecula de mPEG mare, ramificata, continand 2 lanturi identice de 20 KD, care a fost atasata de IFN alfa- 2a pentru a fi creat PEG Interfeonul alfa-2a ( 40 KD ) ( PEGASYS ). Pegylarea proteinelor, folosind un mPEG mare, ramificat, are cateva avantaje majore fata de pegylarea care foloseste mPEG liniar cu molecula mica: protectie mai mare fata de proteoliza, imunogenicitate redusa, scaderea clearanceului, incetinirea filtrarii renale, imbunatatirea eficacitatii ca urmare a cresterii concentratiei si a duratei de actiune. Legatura ce uneste mPEG 40 KD de IFN alfa-2a este o legatura chimica stabila, de tip amidic. Ca o consecinta a acestei legaturi stabile de tip amidic, mPEG de 40 KD nu se detaseaza usor de IFN alfa-2a. De aceea PEG Interferonul alfa-2a este o entitate biologic activa prin ea insasi si nu un prodrog al IFN alfa. In plus PEG Interferonul alfa-2a poate fi conditionat in solutie gata pentru injectare.
 hepatita c" v:shapes="_x0000_i1029">
hepatita c" v:shapes="_x0000_i1029">
. 9. Structura PEG a PEG
Interferonul alfa-2a ( 40 KD ) ( 6 ).
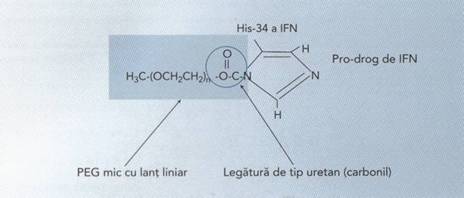
PEG Interferonul alfa-2b ( 12 KD ) ( PegIntron
) este sintetizat printr-o reactie aIFN alfa-2b cu un derivat mPEG
electrofil, carbonat de succinimidil PEG ( SC-PEG ). In procesul de productie
al PEG Interferonului alfa-2b, SC-PEG are potential de
legare cu un numar variabil de aminoacizi din proteina. Acest potential are ca
rezultat PEG Interferonul alfa-2b ( 12 KD ), continand
pana la 13 izomeri de pozitie. Tipul legaturii chimice intre mPEG si proteina
este esentiala si determina multe dintre proprietatile proteinei pegylate.Cea
mai frecventa legatura este cea de tip uretan ( carbonil
) hidrolitic instabila. O consecinta a acestei instabilitati este
aceea ca PEG Interferonul alfa-2b tinde sa actioneze ca un prodrog in sange,
PEG Interferonul alfa-2b se poate depegyla, lasand liber in circulatie IFN
alfa-2b. Din aceleasi motive PEG Interferonul alfa-2b nu este
stabil in solutie si trebuie conditionat ca pulbere liofilizata, aceasta este
reconstituita imediat inainte de injectare.
 hepatita c" v:shapes="_x0000_i1030">
hepatita c" v:shapes="_x0000_i1030">
ura 10. Structura PEG a PEG Interferonului alfa-2b ( 6 ).
Dupa
injectarea subcutanata, IFN alfa conventional este absorbit rapid in
circulatie, cu un timp de injumatatire de absorbtie de doar 2,3
ore. Odata ajuns in circulatie, IFN nemodificat este larg distribuit in
fluidele si tesuturile organismului.Dupa o singura injectie subcutanata de IFN
alfa nemodificat, la o doza de 3 MilU/ml, se obtine in medie o concentratie
maxima de 13,4 UI/ml in aproximativ 10 ore. Timpul de
injumatatire terminal al IFN alfa nemodificat este relativ scurt ( 3-8 ore ) si este principalul factor care limiteaza efectul
terapeutic al acestei molecule. Majoritatea IFN alfa nemodificat ( 70-80% ) este metabolizat rapid si eliminat prin rinichi
desi parte din el poate fi degradat de proteazele nespecifice din sange.
Metabolizarea rapida si eliminarea IFN alfa nemodificat inseamna ca in 24 de
ore ramane prea putin IFN alfa nemodificat in ser, acesta necesitand
administrarea frecventa a dozelor de IFN alfa nemodificat, pentru a obtine o
eficacitate sustinuta.
Ca si IFN alfa nemodificat, PEG Interferonul alfa-2b este absorbit rapid dupa
administrarea prin injectare subcutanata si are un timp de absorbtie de doar 4,6 ore. Odata ajuns in circulatie, PEG Interferonul alfa-2b este larg distribuit in fluidele si tesuturile organismului,
in consecinta volumul sau de distributie este dependent de greutatea corporala
a fiecarui individ. Dozarea in functie de greutate este
recomandata in cazul PEGInterferonul alfa-2b. Dupa o singura injectie
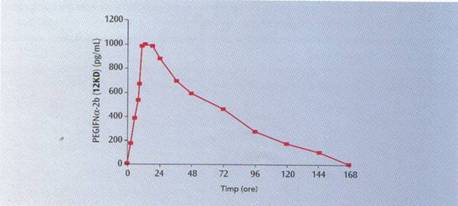
subcutanata de PEGInterferonul alfa-2b,concentratia maxima dureaza intre 15 si
44 de ore dupa care concentratiile plasmatice scad.
 hepatita c" v:shapes="_x0000_i1031">
hepatita c" v:shapes="_x0000_i1031">
. 11. Concentratia serica de PEGInterferon alfa-2b
dupa o singura injectare subcutanata ( 6 ).
Scaderea concentratiilor plasmatice de PEG Interferon alfa-2b la 2-3 zile dupa
administrare sugereaza ca, pentru ultimele 4 zile ale intervalului de dozaj
saptamanal, concentratiile plasmatice de PEG Interferon alfa-2b pot sa nu fie
suficient de mari pentru a mentine supresia virala. 30% din PEG Interferonul
alfa-2b este eliminat renal, restul fiind eliminat
prin catabolism hepatic si degradare dupa interactiunea cu receptorii celulari
ai IFN.
Absorbtia PEGInterferonului alfa-2a este incetinita si mult mai sustinuta decat
cea a IFN alfa nemodificat si aceasta se reflecta in timpul de injumatatire de
absorbtie prelungit ( ~50 de ore fata de 2,3 ore ).
Odata ajuns in circulatie, PEG Interferonul alfa-2a este
distribuit cu precadere in fluxul sangvin si lichidul interstitial dar nu si in
tesuturi. Are de aceea un volum de distributie
restrictionat, similar cu volumul sangvin. Faptul ca PEG Interferonul alfa-2a este distribuit cu precadere in sange are 2 implicatii
foarte importante: in primul rand PEG Interferonul alfa-2a este distribuit
organelor bine irigate, cum este ficatul in al doilea rand PEG Interferonul
alfa-2a nu necesita dozarea in functie de greutatea corporala, o doza standard
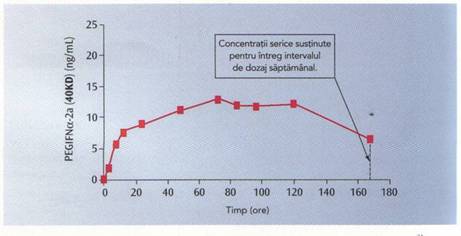
putand fi administrata aproape tuturor pacientilor adulti. O concentratie
maxima medie de 14,2 ng/ml este atinsa in 78 de ore si
este sustinuta timp de 168 de ore.
 hepatita c" v:shapes="_x0000_i1032">
hepatita c" v:shapes="_x0000_i1032">
. 12. Concentratia serica de PEGInterferon alfa-2a dupa o singura injectare subcutanata ( 6 ).
Concentratiile
plasmatice constante de PEG Interferon alfa-2a se ating dupa 5-8 saptamani de
administrare o data pe saptamana iar valoarea concentratiei maxime in acel
moment este de 25,6 ng/ml. Timpul terminal de
injumatatire al PEGInterferonului alfa-2a este mult prelungit ativ cu cel
al IFN alfa nemodificat (~80 de ore fata de 3-8 ore).
PEG Interferonul alfa-2a este cu mult mai putin
metabolizat de catre rinichi si arata o reducere de peste 100 de ori a
clearanceului renal ativ cu IFN alfa nemodificat. PEG Interferonul
alfa-2a este metabolizat in special in ficat fiind
lent degradat de proteazele nespecifice din ficat si sange.
Ribavirina este un analog nucleozidic ce inhiba multiplicarea multor tipuri de virusuri ( inhiba reverstranscriptaza virala). Studiile efectuate au demonstrat ca asociatia Ribavirina Peg Interferon este un tratament mai eficace al infectiei cu virusul hepatitic C decat Peg Interferonul administrat singur.
Contraindicatiile tratamentului cu Ribavirina:
Doza de Ribavirina se stabileste in functie de greutatea corporala:
Principalele efecte adverse ale Ribavirinei sunt: durere
toracica sau tuse persistenta, modificari ale batailor inimii, confuzie,
depresie, parestezii, insomnie, tulburari de gandire sau de concentrare, dureri
epigastrice, scaune melenice sau hematurie macroscopica, epistaxis, febra sau
frisoane care apar dupa cateva saptamani de tratament, dureri lombare, disurie,
algurie, afectiuni oculare sau auditive.
In timpul tratamentului cu Ribavirina se vor monitoriza lunar hemograma,
reticulocitele ( Ribavirina poate da anemie hemolitica
), transaminazele, ureea si creatinina.
Pentru inceput trebuie retinut faptul ca in aceasta afectiune grava,
aveti nevoie de multa odihna si regim alimentar.
Primavara, se poate incepe cu o cura de dovlecei si fasole verde (ciorba,
mancare, salta) deoarece aceste legume contin substante care refac celula
hepatica.Consumati de asemenea multa urda si lapte batut , acestea contin
metionina, o substanta importanta in refacerea celulei hepatice.
Incepeti tratamentul cu pedicuta ,
care contine radium si este foarte eficienta.
Ceaiul de pedicuta se prepara din 1 lingurita de ta,
tocata nu prea marunt, care se pune intr-o cana si
peste care se toarna un sfert de litru de apa clocotita. Se lasa 5 minute
acoperita cana, se strecoara si se bea caldut.
Ceaiul de armurariu se prepara din 1 lingurita si jumatate de
pulbere de armurariu, care se opareste cu o cana cu apa clocotita, se lasa
acoperita 5 minute, se strecoara si se bea.
Polenul granule :
se consuma zilnic 1-3 lingurite inainte de mese.
Tinctura de propolis :
30 de picaturi de tictura se amesteca intr-un pahar cu apa sau ceai, de 3 ori
pe zi, inainte de mese si se beau.
Bitterul suedez :
se foloseste sub forma de comprese pe piele, in dreptul ficatului. Initial se unge bine portiunea de piele cu crema de galbenele, dupa
care se pune compresa imbibata in biter. Se pune seara si se tine cat mai
mult posibil.
Coada calului :
se folosesc comprese imbibate in ceai de coada calului alternativ cu compresele
cu bitter suedez.
Ceai de radacina de patrunjel : se pun 3 radacini de patrunjel la 0.5 l de
apa. Se fierb pana cantitatea de apa scade la jumatate.
Ceaiul se bea caldut. Se bea
numai inainte de masa de dimineata.
Obligeana uscata :
se pune o lingurita de ta intr-o cana de apa si se lasa sa stea peste
noapte. Dimineta se strecoara si lichidul obtinut se
pastreaza la frigider. Se ia de 3 ori pe zi astfel :
3 linguri inainte de masa si 3 linguri dupa masa.
O alta reteta
cu rezultate foarte bune in cazul hepatitei este urmatoarea:
Ingrediente: 3kg morcovi; 3 kg miere de albine, 3 kg lamai, 1
kg frunze de patlagina
Preparare: morcovi se dau pe o razatoare mica, lamaile se taie
marunt, patlagina se fierbe intr-un litru de apa la foc mic pana raane doar o
cana de lichid. Se amesteca toate ingredientele, se pun in
borcane si se pastreaza la frigider. In fiecare dimineata, bolavul va lua cate o lingura pe stomacul gol.
Alimente si preparate permise: paine alba, veche si prajita, paine intermediara, paine Graham fara sare, piscoturi, lapte dulce, lapte batut, lapte [...] |
Untura de porc, slanina, unt si untdelemn prajit, carne grasa de porc, oaie, gasca, rata, vanaturi, mezeluri, maruntaie si viscere, creier, rinichi, c [...] |
Se recomanda alimente bogate in proteine de buna calitate si factori lipotropi: metionina, colina, inozitol si betaina. in perioada de stare a hepati [...] |
Copyright © 2010 - 2025
: eSanatos.com - Reproducerea, chiar si partiala, a materialelor de pe acest site este interzisa!
Informatiile medicale au scop informativ si educational. Ele nu pot inlocui consultul medicului si nici diagnosticul stabilit in urma investigatiilor si analizelor medicale la un medic specialist.
Termeni si conditii - Confidentialitatea datelor - Contact